Оценка эффективности калия и магния аспарагината при профилактике аритмии и возможный механизм антиоксидантного действия
Чжи Яньфан, Хуан Яньшэн, Сюй Боши, Ван Шужэнь
Механизм возникновения аритмии основывается на нарушении электрической активности миокарда, которое тесно связано с дисфункцией различных ионных каналов мембраны кардиомиоцитов, поэтому аритмию также можно рассматривать как один из видов мембранного нарушения. В настоящее время, важным молекулярным механизмом мембранных повреждений считают окислительный стресс. Активные формы кислорода, вступая в цепную реакцию со свободными радикалами, вызывают повреждения и функциональные нарушения молекул липидов и интегральных мембранных белков, что приводит к ряду патологических нарушений, включая повышенную проницаемость мембраны, изменение электрофизиологических свойств мембран и другие. В предшествующих исследованиях нашей группы было обнаружено, что калия и магния аспарагинат улучшает клеточный метаболизм, повышает активность митохондриальной сукцинатдегидрогеназы и цитохромоксидазы, повышает синтез АТФ, усиливает способность сердечной ткани противостоять гипоксии, а также стимулирует активность Na+-K+–АТФазы и способствует захвату K+ и Mg2+ клетками[1]. Калия и магния аспарагинат оказывает благоприятный эффект на функции клеточной мембраны, кроме того данный препарат клинически используется в качестве дополнительной терапии для лечения острого инфаркта миокарда, различных нарушений сердечного ритма, острого и хронического гепатита, поэтому основной целью данного исследования было изучение того, может ли препарат калия и магния аспарагинат предотвратить окислительный стресс при ишемической болезни сердца и аритмии, и связан ли с этим лечебный эффект препарата по отношению к нарушениям сердечного ритма.
1 Материалы и методы
1.1 Выбор пациентов:
Для данного исследования были отобраны 98 пациентов с ишемической болезнью сердца, стенокардией и ишемической аритмией, проходивших лечение в Народной больнице провинции Хэнань в отделении кардиологии, в палатах для руководящих кадровых работников, в период с июля 2005 года по февраль 2006 года. От всех пациентов было получено информированное согласие. Среди пациентов было 64 мужчины и 34 женщины в возрасте от 43 до 94 лет, средний возраст 70,97±10,63; индекс массы тела 17,11–32,28 кг/м2, среднее значение 25,36±3,04 кг/м2. В рамках простого слепого рандомизированного исследования пациенты были разделены на две группы — исследуемую (65 человек) и контрольную (33 человека). При статистическом анализе между группами не было выявлено статистически значимых различий по полу, возрасту и индексу массы тела (P>0,05), поэтому возможно было проводить сравнение.
1.2 Критерии включения и исключения:
у пациентов, включённых в исследование, диагностировали желудочковую и/или наджелудочковую экстрасистолию, вызванную ишемической болезнью сердца; ишемическая экстрасистолия[2] или нестабильная стенокардия[3] диагностированы в соответствии с руководствами. Критерии исключения: атриовентрикулярная блокада 3 степени; синдром слабого синусового узла; синусовая брадикардия тяжёлой степени (частота сердечных сокращений <50 уд./мин); прием антиаритмических средств и препаратов, влияющих на проводимость сердечной мышцы, на момент начала исследования, или прекращение приема таких препаратов менее чем за 5 периодов полувыведения, за исключением β-блокаторов[4]; нарушения вегетативной регуляции сердечной деятельности, боль в груди, вызванная шейным спондилёзом; сопутствующая артериальная гипертензия тяжёлой степени (систолическое давление ≥180 мм рт. ст., диастолическое давление ≥110 мм рт. ст. [1 мм рт. ст. = 0,133 кПа]); тяжёлая сердечная недостаточность и другие серьёзные заболевания, ограничивающие подвижность; заболевания клапанов сердца и другие заболевания сердца, вызывающие стенокардию; сопутствующие тяжёлые нарушения функции печени, почек (креатинин >176,8 мкмоль/л), заболевания системы кроветворения, эндокринные и метаболические заболевания, заболевания соединительной ткани, опухоли; содержание калия в крови >5,5 ммоль/л; другие факторы, которые по мнению исследователей препятствуют участию в клиническом исследовании.
1.3 Применение препаратов:
пациенты контрольной группы принимали только стандартные препараты для лечения сердечно-сосудистых заболеваний и не принимали калия и магния аспарагинат в форме раствора для инъекций. Пациенты исследуемой группы, в дополнение к стандартной терапии сердечно-сосудистых заболеваний, применяли препарат Панангин в форме внутривенной инфузии в дозе 30 мл в 250 мл 5 % раствора глюкозы (у пациентов с сахарным диабетом раствор глюкозы заменяли физиологическим раствором). В период исследования не разрешалось применение витамина С, В, коэнзима Q и других лекарственных препаратов, которые влияют на окислительно-восстановительные реакции; в отношении препаратов стандартной терапии между двумя группами в максимально возможной степени поддерживалось равновесие, чтобы обеспечить сравнимость контрольной и исследуемой групп.
1.4 Отбор и хранение образцов крови, и измерение концентрации малондиальдегида (МДА), окисленных липопротеинов низкой плотности (окЛПНП):
перед началом лечения и через 1 неделю после начала терапии у пациентов ранним утром натощак отбирали 3 мл венозной крови в пробирку с предварительно охлаждённым гепарином (187,5 Ед/0,3 мл) в качестве антикоагулянта для хранения в холодильнике при температуре 2–8 C. После хранения при низкой температуре (ниже 4 С) в течение 30 мин проводилось центрифугирование крови (радиус = 7 см) в течение 5 минут на скорости 5000 об/мин. После этого плазму крови разделяли на аликвоты по 0,5 мл и хранили в центрифужной пробирке (пробирка ЕР) в морозильной камере (при температуре –30 С). Концентрацию МДА определяли колориметрическим методом с помощью тиобарбитуровой кислоты. Все используемые реагенты были изготовлены в Биологическом институте города Нанкин, исследования проводились согласно инструкции. Концентрацию окЛПНП определяли с помощью твердофазного иммуноферментного анализа (ELISA). Набор реагентов был изготовлен Даляньской компанией по разработке химических реагентов «Фаньбан», исследования проводились согласно инструкции.
1.5 Определение концентрации восстановленного глутатиона (GSH) и окисленного глутатиона (GSSG):
к 0,5 мл плазмы крови добавляли 0,5 мл 10 % раствора метафосфорной кислоты, далее проводили центрифугирование (радиус=7 см) при низкой температуре (ниже 4 С) в течение 20 минут при скорости 5000 об/мин и собирали 0,5 мл надосадочной жидкости, которую переносили в пробирку ЕР и хранили в морозильной камере, таким образом подготовив к измерению концентрации GSH и GSSG. Метод приготовления стандартного раствора GSH приведён в таблице 1; метод приготовления стандартного раствора GSSG идентичен GSH, для разведения используют 0,1 М раствор NaOH. Для оценки концентрации GSH в 100 мкл подготовленной плазмы крови добавляли 900 мкл 0,1 М раствора NaHPO2, содержащего 0,005М этилендиаминтетрауксусной кислоты (ЭДТА); для измерения концентрации GSSG в плазму крови добавляли 900 мкл 0,1 М раствора NaOH. После тщательного перемешивания к 100 мкл полученного раствора добавляли 1900 мкл соответствующего буферного раствора и 100 мкл орто-фталальдегида (ОФА) в метаноле. После тщательного перемешивания раствор оставляли на 30 минут. Интенсивность флуоресценции оценивали при длине волны возбуждения 334,4 нм и длине волны излучения 422,4 нм.

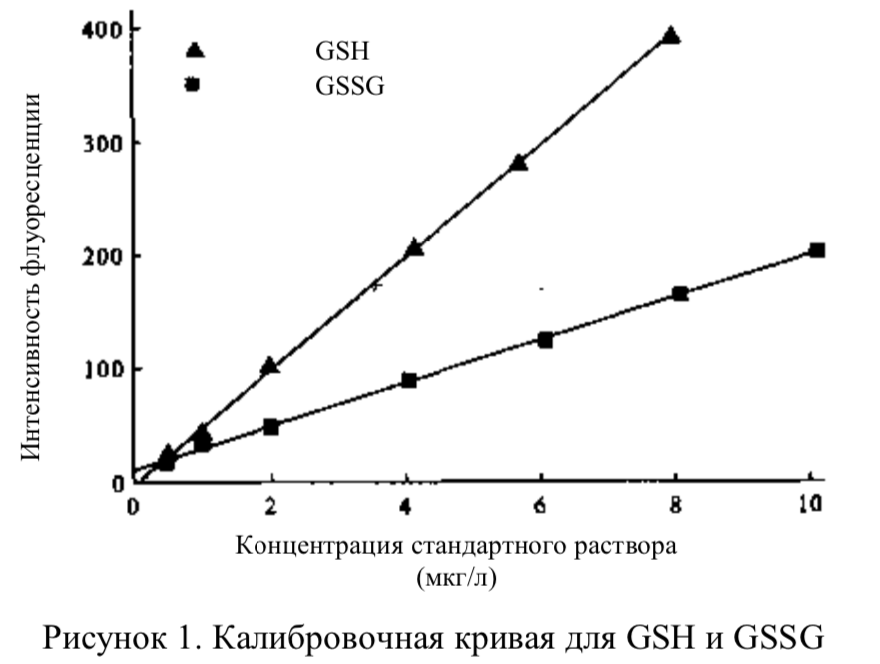
В данной таблице «0» обозначает пустую пробирку, концентрация стандартного раствора GSH в пробирках 1-7 составляет 0,5, 1, 2, 4, 6, 8 и 10 мг/л соответственно. После добавления ОФА в метаноле в концентрации 1 г/л растворы перемешивали и оставляли на 30 минут при комнатной температуре. Интенсивность флуоресценции оценивали при длине волны возбуждения 334,4 нм и длине волны излучения 422,4 нм. По результатам изменений строится калибровочная кривая, где по оси абсцисс указывают концентрацию стандартного раствора, по оси ординат — интенсивность флуоресценции (см. рисунок 1). Калибровочная кривая для GSH: y=44,670 8x–1,693 1 (r=0,998, P=0,000); калибровочная кривая для GSSG: y=15,095 8x+1,248 6 (r=0,997, P=0,000); r — коэффициент регрессии, результаты показывают хорошую линейную зависимость.
1.6 Клиническое наблюдение:
перед началом приема препарата и после приема препарата в течение 1 недели кроме оценки показателей окислительного стресса проводили измерение артериального давления, общий анализ мочи, крови и кала, оценивали показатели функции печени, электролиты, креатинин в сыворотке крови, мочевую кислоту, глюкозу и липиды крови, миокардиальные ферменты и др. У пациентов с аритмией проводился непрерывный 24-часовой мониторинг сердечного ритма до лечения и через 1 неделю лечения.
1.7 Статистический анализ:
стандартные растворы и все образцы исследовали параллельно, среднее число считалось за фактическое значение для данных образцов. Для проведения статистического анализа использовали программу SPSS12.0, данные измерений выражали в виде среднего ± стандартное отклонение(x̅ ±s),для сравнения 2 показателей использовали t-критерий Стьюдента и линейный корреляционный анализ. Различия считали достоверными при P<0,05.
2 Результаты исследования
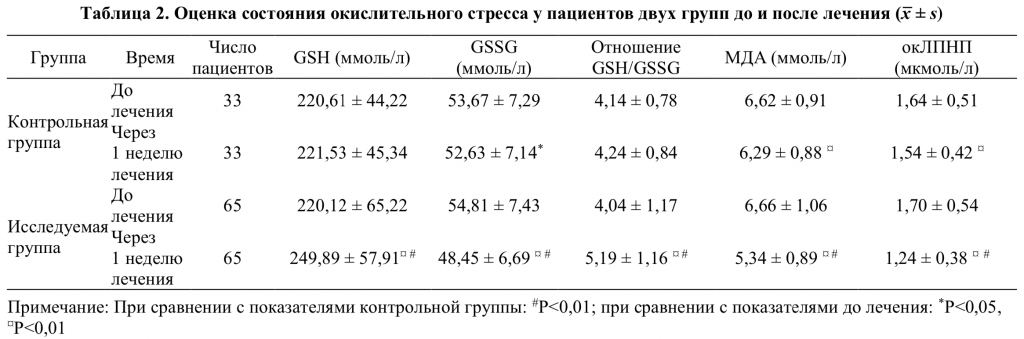
2.1 Терапевтический эффект калия и магния аспарагината на окислительный стресс (таблица 2):
До начала лечения между группами не выявлено статистических различий (P>0,05). После приема препарата в течение 1 недели у пациентов исследуемой группы концентрация GSH повысилась на 13,52 %, концентрация GSSG снизилась на 11,59 %, отношение GSH/GSSG повысилось на 28,71 %, концентрация МДА понизилась на 19,69 %, концентрация окЛПНП понизилась на 27,02 %; отмечаются статистически значимые различия по сравнению с показателями до начала лечения (P<0,01). У пациентов контрольной группы концентрация GSH повысилась на 0,42 %, концентрация GSSG снизилась на 1,93 %, отношение GSH/GSSG повысилось на 2,56 %, концентрация МДА понизилась на 5,02 %, концентрация окЛПНП понизилась на 6,47 %; динамика улучшения каждого показателя значимо менее выражена, чем в исследуемой группе (P<0,01).
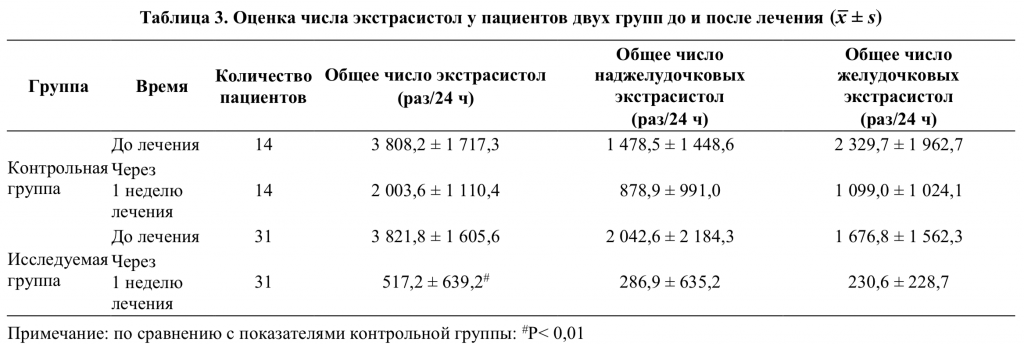
2.2 Терапевтический эффект калия и магния аспарагината в отношении экстрасистолии (таблица 3):
При сравнении общего числа экстрасистол у пациентов двух групп до начала лечения статистических различий не выявлено. Через 1 неделю лечения число экстрасистол у пациентов двух групп значимо снизилось, однако степень снижения достаточно сильно различалась. Количество экстрасистол у пациентов исследуемой группы уменьшилось на 86,5 %, общее число желудочковых экстрасистол уменьшилось на 86,2 %, число наджелудочковых экстрасистол сократилось на 86,0 %; однако, у пациентов контрольной группы количество экстрасистол уменьшилось на 47,4 %, общее число желудочковых экстрасистол уменьшилось на 52,8 % и общее число наджелудочковых экстрасистол сократилось на 40,6 %.
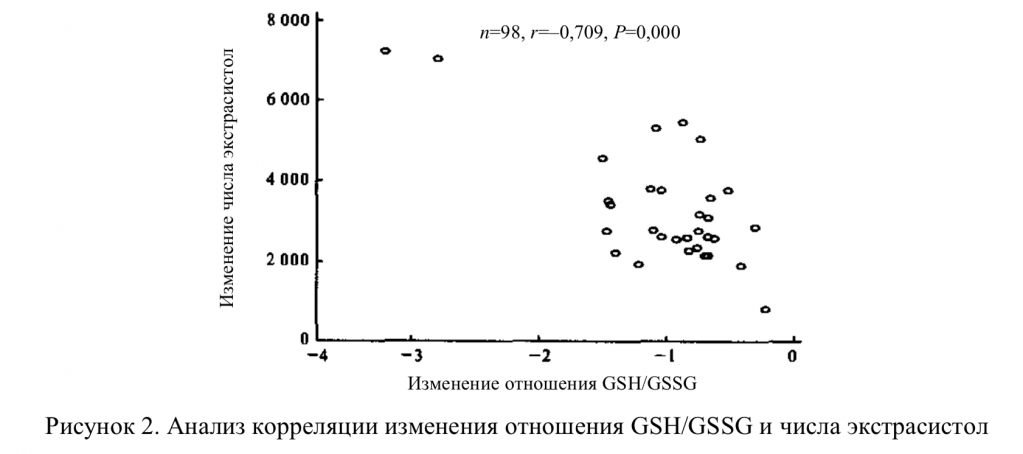
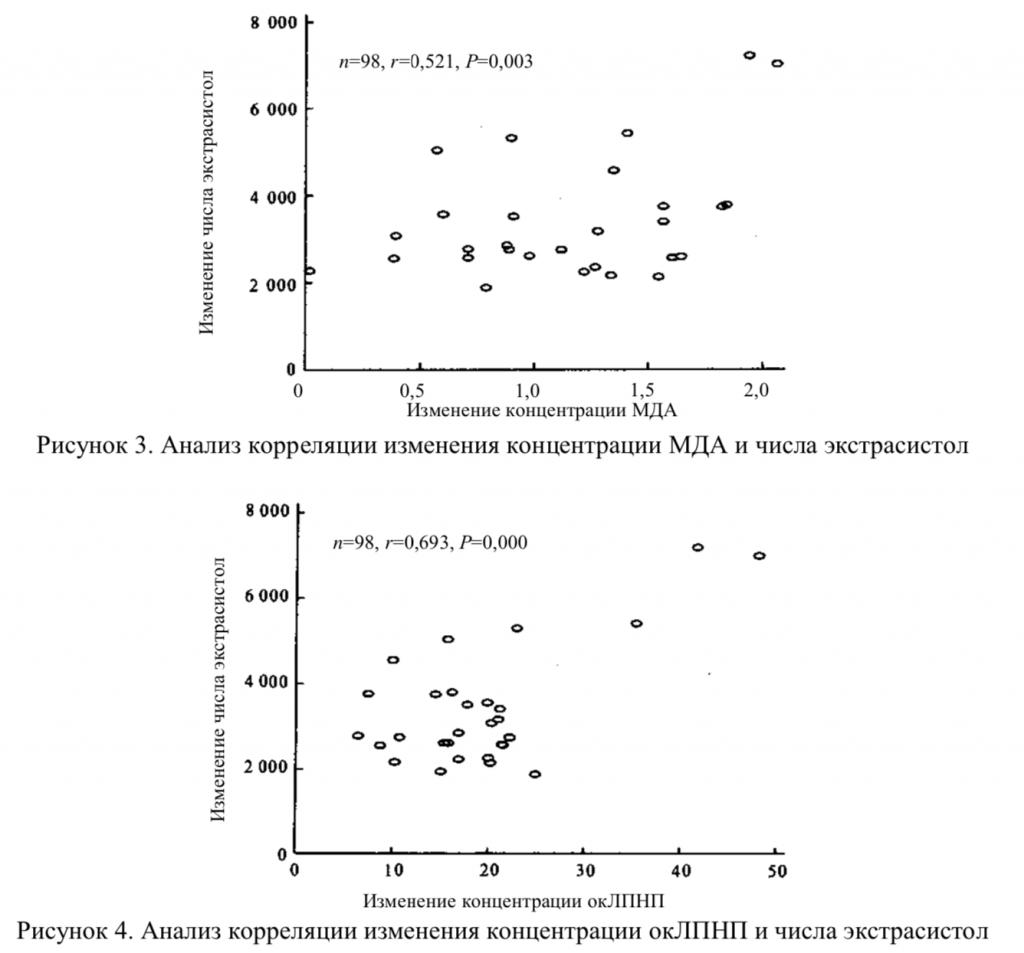
2.3 Корреляционный анализ показателей терапевтического действия калия и магния аспарагината на частоту возникновения экстрасистол и состояние окислительного стресса (рис. 2–4):
исходя из тенденции изменения вышеуказанных данных, между показателями терапевтического эффекта калия и магния аспарагината на частоту возникновения экстрасистол и состояние окислительного стресса отмечается высокая согласованность (P<0,01), в особенности для взаимосвязи между отношением GSH/GSSG, концентрацией окЛПНП и снижением числа экстрасистол, что указывает на то, что окислительный стресс может играть важную роль в развитии аритмии.
2.4 Нежелательные явления:
при тщательном наблюдении за симптомами заболевания и изменением состояния в период лечения не было выявлено случаев возникновения побочных эффектов и токсического действия, также не было зафиксировано значимых изменений функции почек и печени, биохимических показателей крови и миокардиальных ферментов при приёме препарата Панангин.
3 Обсуждение
3.1 Выбор показателей окислительного стресса:
активные формы кислорода могут вызывать обширные повреждения различных структур и компонентов тканей. Липиды, белки, нуклеиновые кислоты, витамины и другие жизненно важные компоненты являются мишенью активных форм кислорода, вследствие чего происходит образование других свободных радикалов. Исследования показывают, что для оценки уровня окислительного стресса часто используют карбонил в качестве индикатора степени окислительного повреждения белков на ранней стадии[5]. Конечные продукты окисления (АоРР) и конечные продукты гликирования (AGE) белка часто применяют в качестве показателей поздней стадии окислительных разрушений белка[6]. Концентрация МДА отражает степень окислительного повреждения липидов; окЛПНП являются общепризнанными показателями окислительного разрушения липидов крови; считается, что повышение их уровня тесно связано с развитием атеросклероза[7]. Они также являются одними из важнейших индикаторов, отражающих общий уровень окислительного разрушения липидов в организме.
Состояние окислительного стресса в организме зависит от окислительно-восстановительного баланса, который также называется «редокс-статус»[8]. В настоящее время обнаружено, что поддержание данного баланса обеспечивает множество биомакромолекул. Отношение GSH/GSSG является самым главным регулятором эндогенных окислительно-восстановительных реакций организма, поэтому содержание GSH намного превышает уровень других антиоксидантов; кроме того, отношение GSH/GSSG регулируется несколькими механизмами[9]. По этой причине, в качестве главного индикатора состояния окислительного стресса в организме в данном исследовании было выбрано отношение GSH/GSSG.
3.2 Возможные механизмы снижения окислительного стресса под действием калия и магния аспарагината:
скорее всего, механизм антиоксидантного действия калия и магния аспарагината главным образом связан с содержанием ионов магния (Mg2+). Перенасыщение ионами железа (Fe2+) является одной из главных причин окислительного стресса в организме, и в настоящее время считается, что перенасыщение Fe2+ происходит по кальциевым каналам L-типа (LVDCC), а ионы Mg2+ как раз являются их природным блокатором[10]. Костеллоу и соавт.[11] исследовали воздействие внеклеточных ионов магния на катализируемое железом окисление липидов на препаратах аорты крыс и гладкомышечных клеток артерий человека и обнаружили, что когда концентрация ионов магния в питательной среде, содержащей ионы железа, снизилась с физиологического показателя до патологического (0,3–05 ммоль/л), содержание продуктов окисления фосфолипидов МДА и 4-гидроксиалкеналя (4-ГА) повысилось в 2–3 раза, а уровень внеклеточного глутатиона понизился. При увеличении концентрации Mg2+ уровень МДА/4-ГА снизился, а уровень внеклеточного глутатиона повысился, что свидетельствует о защитном действии Mg2+ на катализируемое Fe2+ перекисное окисление липидов клеточной мембраны, и соответственно о протекторном действии Mg2+ при сердечно-сосудистых заболеваниях. Защитная функция внеклеточного магния связана с его способностью поддерживать достаточную концентрацию глутатиона, повышая уровень GSH. GSH предотвращает катализируемое ионами перекисное окисление липидов, снижает уровень внутриклеточных сфинголипидов и церамидов, ингибирует транскрипционный фактор κB (NF-κB), ингибирует активность фактора некроза опухоли альфа (ФНО-α), интерлейкина6 (ИЛ-6), ИЛ-8, макрофагального воспалительного белка2 (MIP-2), моноцитарного хемотаксического белка1 (MCP-1) и других воспалительных цитокинов, а также снижает воспаление при сердечно-сосудистых заболеваниях[12–13]. Недостаток магния может увеличить число свободных радикалов, что связано с риском развития инфаркта миокарда, так как при этом повышается степень окислительного повреждения миокарда[14]. При недостатке магния в организме может повышаться длительность «оглушения» миокарда, усиливаться окислительное повреждение и снижаться сердечная функция[15]. Кроме того, недостаток магния может привести к увеличению концентрации супероксидных анионов и нейропептидов, вследствие чего нейропептиды индуцируют пролиферацию сердечных фибробластов через механизмы, опосредованные супероксид-анионом, что приводит к фиброзу миокарда[16]. Магний ингибирует оксидазу восстановленного коэнзима II (NADPH), снижая продукцию супероксидных анионов, при этом его действие эквивалентно эффекту других сильнодействующих ингибиторов оксидазы NADPH. Применение магния значимо повышает активность супероксиддисмутазы и пероксидазы, концентрацию глутатиона и усиливает захват свободных радикалов. Кроме того, антагонизм магния и кальция приводит к снижению эндогенной продукции оксида азота (NO) и пероксинитритов, уменьшая повреждение миокарда[17].
3.3 Механизм протекторного действия калия и магния аспарагината в отношении аритмии может быть связан с его антиоксидантным действием:
многочисленные исследования окислительного стресса при аритмии в основном сосредоточены на механизме возникновения фибрилляции предсердий. Согласно сообщению Лина и соавт.[18], у пациентов с фибрилляцией предсердий наблюдается значительное окислительное повреждение митохондриальной ДНК, а уровень 8-оксо-2′-дезоксигуанозина (8-OHdG) значимо повышен по сравнению с пациентами, не страдающих этим заболеванием. По мнению авторов, окислительное повреждение митохондрий может усугубить нарушение энергетического обмена и окислительный стресс и в конечном итоге привести к образованию замкнутого круга. Коранзопулос и соавт.[19] считают, что окислительный стресс способствует электрическому ремоделированию миокарда, вызывая изменения электрофизиологических характеристик миокарда и хроническую фибрилляцию предсердий. Чжу Юаньцзюнь и соавт.[20] также продемонстрировали протекторное действие калия и магния аспарагината в условиях гипоксии на изолированном сердце. Используемые препараты магниевой и калиевой соли аспарагиновой кислоты показали большую аффинность к клеткам, чем другие продукты калия и магния аспарагината, состоящие из аспарагиновой кислоты, калия хлорида и магния сульфата, при этом ионы магния и калия могут успешно проникать внутрь клетки и использоваться, оказывая терапевтическое действие.
Результаты данного исследования показали, что калия и магния аспарагинат значимо снижает частоту экстрасистол и улучшает оксидативный статус у больных ишемической болезнью сердца, и между этими двумя эффектами существует выраженная корреляция. Хотя описанные выше результаты не являются прямым доказательством, однако они указывают на то, что состояние окислительного стресса может быть важным механизмом патогенеза экстрасистолии при ишемической болезни сердца. Применение антиоксидантов для лечения экстрасистолии требует дальнейшего исследования. Калия и магния аспарагинат может быть не только вспомогательным средством для профилактики аритмии, его антиоксидантные свойства также могут помочь защитить кардиомиоциты и их восстановить электрофизиологические свойства.
1 Пэн Кэцзюнь, Ван Цюлинь, У Чэньхэн, и другие. Влияние калия и магния аспарагината на метаболизм гепатоцитов (J). Китайский журнал о новых препаратах, 2005, 24 (3): 215 – 219.
2 Чэнь Гуйянь, Сюэ Сайцинь. Новейшие внутренние и международные стандарты диагностики и лечения заболеваний (M). Пекин: Издание Сюэюань, 1992: 220 – 223.
3 Медицинская ассоциация Китая, филиал изучения сердечно-сосудистых заболеваний, Редакционный комитет Китайского журнала кардиологии. Диагностика и рекомендации по лечению нестабильной стенокардии (J). Китайский журнал кардиологии, 2000, 28 (6): 409 – 412.
4 Исследовательская группа OASIS: Лян Янь, Тань Хуэйюн, Чжу Цзюнь и другие. Анализ факторов риска внезапной смерти или смерти от аритмии у пациентов с острым коронарным синдромом без подъёма сегмента ST [J]. Китайский журнал реаниматологии, 2005, 17 (3): 142 – 145.
5 Dalle-Donne I, Rossi R, Giustarini D, et al. Protein carbonyl groups as biomarkers of oxidative stress (J). Clin Chim Acta, 2003, 329 (1 – 2): 23 – 38.
6 Ван Цюлинь, Ван Хаои, Ван Шужэнь. Оценка состояния окислительного стресса (J). Китайский журнал патофизиологии, 2005, 21 (10): 2069 – 2074.
7 Brigelius-Flohe R, Maurer S, Lotzer K, et al. Overexpression of PHGPx inhibits hydroperoxide-induced oxidation, NFkappaB activation and apoptosis and affects oxLDL-mediated proliferation of rabbit aortic smooth muscle cells (J). Atherosclerosis, 2000, 152 (2): 307 – 316.
8 Seyfried J, Evert B O, Schwarz C S, et al. Gene dosage-dependent effects of bcl-2 expression on cellular survival and redox status (J). Free Radic Biol Med, 2003, 34 (12): 1517 – 1530.
9 Hogg P J. Disulfide bonds as switches for protein function (J). Trends Biochemical Sciences, 2003, 28 (4): 210 – 214.
10 Oudit G Y , Sun H, Trivieri M G, et al. L-type Ca2+ channels provide a major pathway for iron entry into cardiomyocytes in iron-overload cardiomyopathy (J). Nat Med, 2003. 9 (9): 1187 – 1194.
11 Kostellow A B, Morrill G A. Iron-catalyzed lipid peroxidation in aortic ceils in vitro: protective effect of extracellular magnesium (J). Atherosclerosis, 2004, 175 (1): 15 – 22.
12 Levade T, Auge N, Veldman R J, et al. Sphingolipid mediators in cardiovascular biology and pathology (J). Cire Res, 2001, 89 (11): 957 – 968.
13 Хуан Чжунвэй, Тан Цзяньчжун, Чэнь Юй и другие. Протекторное действие восстановленного глутатиона при полиорганной недостаточности у пациентов с острым панкреатитом (J). Китайский журнал реаниматологии, 2005, 17 (11): 673 – 674.
14 Kharb S, Singh V. Magnesium deficiency potentiates free radical production associated with myocardial infarction (J). J Assoc Physicians India, 2000, 48 (5): 484 – 485.
15 Tang W, Weil M H, Sun S, et al. The effects of biphasic and conventional monophasic defibrillation on postresuscitiation myocardial function (J). J Am Coll Cardiol, 1993, 34 (3): 815 – 822.
16 Kumaran C, Shivakumar K, Superoxide-mediated activation of cardiac fibroblasts by serum factors in hypomagnesemia (J). Free Radical Biol Med, 2001, 31 (7): 882 – 886.
17 Zhang Y, Davies L R, Martin S M, et al. Magnesium reduces free radical concentration and preserves left ventricular function after direct current shocks (J). Resuscitation, 2003, 56 (2): 484 – 485.
18 Lin P H , Lee S H, Su C P, et al. Oxidative damage to mitochondrial DNA in atrial muscle of patients with atrial fibrillation (J). Free Radic Biol Med, 2003, 35 (10): 1310 – 1318.
19 Korantzopoulos P, Kolettis T, Siogas K, et al. Atrial fibrillation and electrical remodeling: the potential role of inflammation and oxidative stress (J). Med Sci Monit, 2003, 9 (9): RA225 – 229.
20 Чжу Юаньцзюнь, Су Лян, Чжан Куй и другие. Протекторное действие калия и магния аспарагината в условиях гипоксии изолированного сердца (J). Китайский журнал клинической фармакологии, 2006, 15 (2): 90 – 92.
Финансирование проекта: Программа финансирования докторантуры Министерства образования (20050610050)
Организация автора: 610041, провинция Сычуань, город Чэнду, Сычуаньский университет, Институт фундаментальной и судебной медицины, Кафедра патологических и физиологических процессов (Чжи Яньфан, Хуан Яньшэн, Ван Шужэнь); 450003, провинция Хэнань, город Чжэнчжоу,
Центральная лаборатория Народной больницы провинции Хэнань (Сюй Боши)
Ответственный автор: Ван Шужэнь, научный руководитель докторантов (Email: wangshuren1945@yahoo.com.cn)
Информация об авторе: Чжи Яньфан (род. 1980), национальность — хань, родилась в провинции Хэнань, является студенткой магистратуры, в основном занимается исследованиями патофизиологии сердечно-сосудистых заболеваний.
(Дата получения исходного текста статьи: 25.03.2007 г. Дата редакции: 14.08.2007 г.) (Редактор статьи: Ли Иньпин)
http://www.cqvip.com Chin Crit Care Med, November 2007, Vo1.19, No.11