Гипокалиемия и гипомагниемия и их коррекция у детей и подростков
Козловский А.А., Гомельский государственный медицинский университет

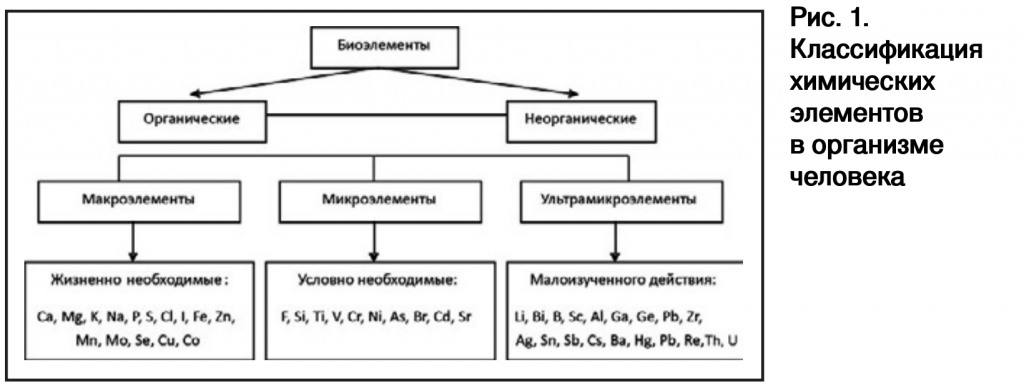
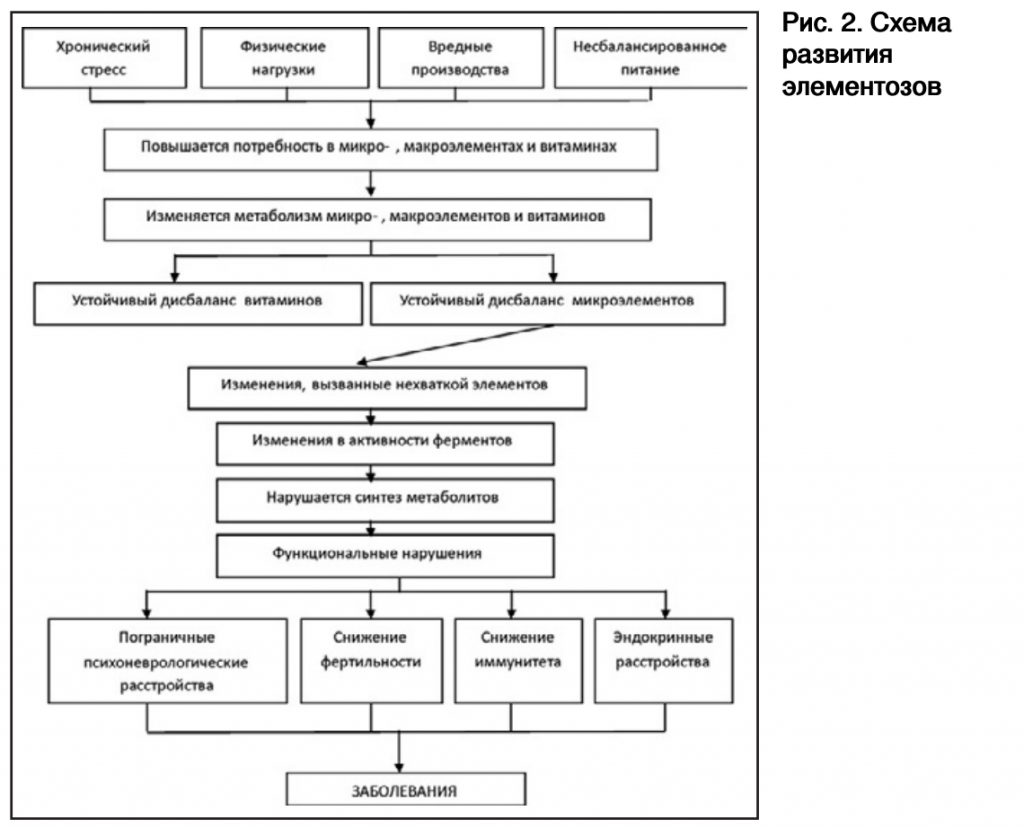
Минеральные вещества необходимы для обеспечения нормальной жизнедеятельности организма. Они поддерживают постоянство внутренней среды, кислотно-щелочное равновесие, водносолевой обмен. Практически все химические элементы периодической таблицы Д.И. Менделеева участвуют в физиологических и патологических процессах человека. Организм человека на 60% состоит из воды, на 34% – из органических веществ и на 6% – из неорганических веществ. Органические элементы, из которых формируется наша органическая составляющая, – углерод, водород, кислород, азот, фосфор, сера. В неорганической составляющей обязательно присутствуют 22 химических элемента: Ca, P, O, Na, Mg, S, B, Cl, K, V, Mn, Fe, Co, Ni, Cu, Zn, Mo, Cr, Si, I, F, Se; 12 компонентов в организме человека являются структурными, так как они на 99% формируют его элементный состав: C, O, H, N, Ca, Mg, Na, K, S, P, F, Cl. Все представленные химические элементы можно разделить на жизненно необходимые (эссенциальные), условно необходимые и элементы, роль которых до настоящего времени еще недостаточно изучена (рис. 1). Эссенциальные химические элементы – это элементы, при отсутствии или недостатке которых нарушается нормальная жизнедеятельность организма [15]. Ученые давно обратили внимание на то, что многие болезни связаны с недостатком того или иного химического элемента в организме (гипоэлементоз). Минералы и металлы в лечебных целях применяли в Древнем Китае, Индии, Месопотамии. В Британской фармакопее середины XIX в. представлены тысячи лекарственных средств, содержащих химические элементы [30]. Гипоэлементоз может стать причиной не только временных нарушений в организме, но и способствовать развитию серьезных заболеваний [13]. Схема развития элементозов представлена на рис. 2. В последние годы возрастает интерес к изучению биологической роли макро- и микроэлементов.
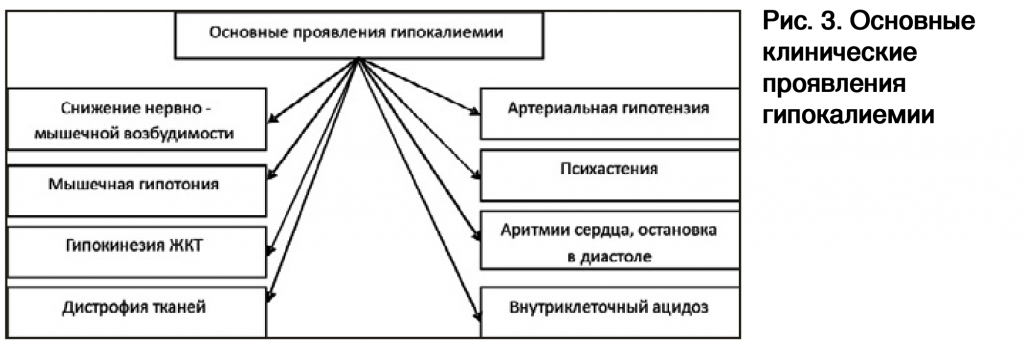
Особое внимание неслучайно уделяется калию и магнию как одним из наиболее распространенных в человеческом организме. Калий и магний в ионизированной форме представляют собой положительные ионы – катионы, соответственно с одним (К+ ) и двойным положительными зарядами (Mg2+). Это одни из самых распространенных элементов на Земле. Особенно много калия и магния в воде Мирового океана, электролитный состав которой близок к электролитному составу сыворотки крови [14]. Калий – основной внутриклеточный катион тканей различных органов, примерно 98% его сосредоточено внутри клеток. В условиях нормы в клетке его содержится 150–160 ммоль/л, а в сыворотке крови – 3,7– 5,5 ммоль/л. Большая часть калия в организме находится внутриклеточно, поэтому возможна существенная потеря внутриклеточного калия без больших изменений его содержания в сыворотке. Натрий-калиевый насос, расположенный в клеточной мембране, – основной механизм поддержания баланса между внутри- и внеклеточным калием. Ион калия – весьма важный компонент в поддержании гомеостаза, особенно в критических состояниях. Калий играет существенную роль в осуществлении биоэлектрической активности клеток и поддержании нервно-мышечной возбудимости и проводимости. В нормальных условиях калий поступает с пищей и абсорбируется через желудочно-кишечный тракт (ЖКТ) с последующей экскрецией избытка через почки. Эффективному усвоению калия способствует витамин В6 , а алкоголь, наоборот, оказывает негативное влияние на баланс этого элемента [1]. Суточная потребность ребенка в калии зависит от возраста: 1–3 года – 400 мг, 3–7 лет – 600 мг, 7–11 лет – 900 мг, 11–14 лет – 1500 мг, старше 14 лет – 2500 мг. Высокое содержание калия отмечается в кураге, урюке, фасоли, черносливе, горохе, орехах, щавеле, картофеле, шпинате, петрушке, черной смородине, абрикосах и колеблется от 1780 до 300 мг% (продукты указаны в порядке убывания содержания калия). Гипокалиемия – стойкое снижение сывороточной концентрации калия (менее 3,5 ммоль/л). Организм взрослого человека весом в 70 кг содержит 136,85 г или 3500 ммоль калия. Причины развития гипокалиемии: 1. Недостаточное (менее 10 мэкв/ сут) поступление калия в организм с пищей (при голодании или ограничении приема продуктов, содержащих калий). 2. Избыточное выведение калия из организма в результате: – хронических профузных поносов (кишечные секреты содержат большое количество калия); – многократной рвоты (содержание калия в желудочном соке невысокое, однако развитие гиповолемии вызывает вторичный гиперальдостеронизм и увеличение экскреции ионов К+ почками); – повышенного выведения калия почками при неправильном применении диуретиков, первичном и вторичном гиперальдостеронизме, дефектах почечных канальцев (синдром Барттера, почечный канальциевый ацидоз), повреждении почечной ткани нефротоксическими веществами, в том числе лекарственными препаратами (пенициллинами, гентамицином, амфотерицином В), гипомагниемии (способствует не только выходу калия из клеток, но и увеличивает его экскрецию с мочой). 3. Перераспределение ионов калия из крови и/или межклеточной жидкости в клетки в условиях: – увеличения уровня инсулина в крови; – гиперкатехоламинемии (в результате применения препаратов адреналина, норадреналина, дофамина, при феохромоцитоме, остром стрессе); – передозировки фолиевой кислоты или витамина В (указанные вещества стимулируют пролиферацию клеток и потребление ими ионов калия). Симптоматика нарушений калиевого гомеостаза зависит от его содержания в организме (при этом концентрационные показатели калия в плазме неточно отражают состояние калиевого баланса, хотя и имеют достаточно узкий предел колебаний). Основные проявления гипокалиемии связаны с нарушением электрических свойств мембран возбудимых тканей. Жалобы и симптомы, сопровождающие снижение уровня калия в организме, разнообразны и неспецифичны, что позволяет говорить не о клинической картине, а о многочисленных клинических масках гипокалиемии. Самые частые из них – нейромиопатические и психоэмоциональные нарушения, кардиальный синдром, синдром полиурии-полидипсии (рис. 3). Дисбаланс калия приводит к нарушению поляризации и деполяризации клеточных мембран, нарушению функции фолинэстеразы. Главный результат этих сдвигов – расстройство процесса передачи возбуждения с нерва на мышцу, что клинически выражается усталостью, мышечной слабостью, спазмами мышц ног, парестезиями в области конечностей, угасанием сухожильных рефлексов [23]. Неспецифические симптомы гипокалиемии – потеря аппетита, потеря концентрации, апатия. Гипокалиемия проявляется также расстройствами сердечно-сосудистой деятельности, характеризующимися угнетением сократительной функции миокарда, возникновением систолического шума на верхушке сердца и расширением его полостей, снижением артериального давления [22]. Применительно к гастроэнтерологии и урологии это означает, что поражение гладкой мускулатуры ведет к парезу кишечника, ослаблению кишечных шумов, рвоте, метеоризму, запорам, атонии мочевого пузыря [18]. Кардиоповреждающее действие дефицита ионов калия в организме рано отражается на ЭКГ, в связи с чем ее можно использовать в качестве индикатора скрытой гипокалиемии. Постоянные, хотя и неспецифическиеи ЭКГ-признаки – частые желудочковые экстрасистолы, пролонгация QRS, снижение сегмента ST, депрессия или инверсия зубца Т, выраженный зубец U. Особенно чувствительны к гипокалиемии больные, принимающие сердечные гликозиды [3, 17].
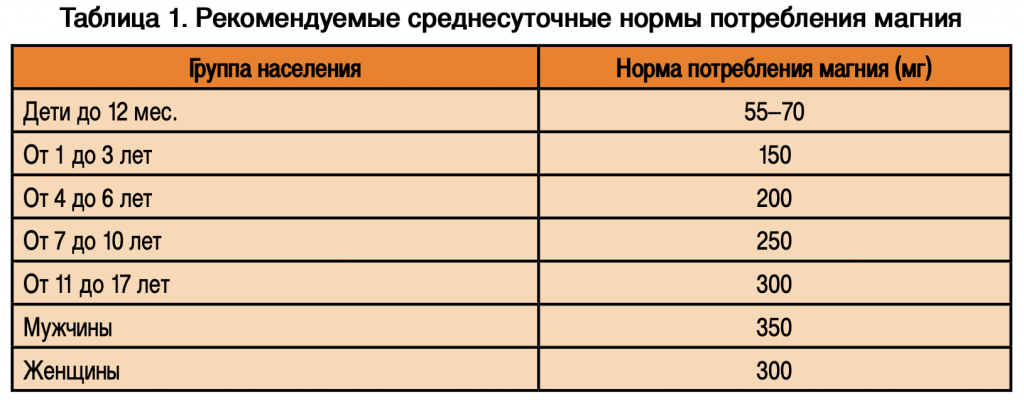
Хроническая гипокалиемия сопровождается функциональным и структурным повреждением центральной и периферической нервной системы. Дисфункция ЦНС реализуется психоэмоциональными расстройствами в форме неглубокого астенического, тревожно-депрессивного или ипохондрического синдромов. Полиморфные сенсорные нарушения представлены легкими парестезиями лица и конечностей либо утратой болевой и тактильной чувствительности или же, напротив, выраженной гиперестезией. Нейромоторные симптомы обычно коррелируют с глубиной и длительностью гипокалиемии, варьируя от слабости мышц конечностей и низких сухожильных рефлексов до общего паралича, включая дыхательные мышцы [6]. Нейровегетативные расстройства имеют преимущественно симпато-адреналовую окраску и могут быть представлены тремором, гипергидрозом, спонтанной эритродермией. Диагностические тесты для определения гипокалиемии: – концентрация калия в сыворотке менее 3,5 ммоль/л – ориентировочный тест; – содержание калия в моче: значения более 20 ммоль/л говорят о потерях калия почками, а менее 20 ммоль/л – о внепочечных причинах калиевого дефицита в плазме; – чресканальцевый градиент концентрации калия, определяемый как произведение отношения калия мочи к калию сыворотки и отношения осмоляльности сыворотки к осмоляльности мочи, выявляет причину повышенного содержания калия в моче; – газы артериальной крови (метаболический алкалоз чаще ассоциируется с гипокалиемией вследствие назогастрального зондирования, диуретической терапии, гиперальдостеронизма, а гиперкалиемия сопутствует и метаболическому ацидозу при диарее, почечном канальцевом ацидозе); – электрокардиография (характерны снижение сегмента ST, уплощение зубца Т, наличие зубца U, желудочковые аритмии). Оценку изменения содержания калия в крови нецелесообразно проводить отдельно от показателей магния, так как магний является важным кофактором как усвоения калия, так и обеспечения его оптимального внутриклеточного уровня. В 1992 г. было доказано, что одновременный дефицит калия и магния может приводить к гипокалиемии, резистентной к лечению, если не проводить коррекцию дефицита магния [10]. Магний не синтезируется в организме человека, а в виде иона Mg2+ поступает с пищей, водой и солью. В природе он занимает 8-е место по распространенности; магнием насыщена морская вода, он является составной частью более 200 минералов, входит в состав хлорофилла. Ежедневная потребность в магнии на 40% удовлетворяется за счет продуктов, на 60% – за счет ионизированного магния воды. Биологическая доступность магния из питьевой воды значительно выше, чем из твердой пищи [11]. Поскольку во многих географических регионах в питьевой воде и почве определяют низкое содержание магния, концентрация элемента в растительных продуктах зависит от места произрастания растений. В индустриально развитых странах технология сельского хозяйства и производства продуктов питания, изменение образа жизни способствуют потере магния и увеличению численности населения с магниевым дефицитом [14]. Высокое содержание магния (от 540 до 102 мг%) отмечают в кунжуте, пшеничных отрубях, семенах подсолнечника, орехах, сое, гречневой крупе, овсяных хлопьях, горохе, кураге, сушеном черносливе (продукты указаны в порядке убывания содержания магния). По данным Института питания РАМН, потребность в магнии взрослого человека составляет 300–400 мг/сут. В молодом возрасте, а также у лиц, занимающихся физическим трудом, у спортсменов потребность в магнии выше. Рекомендуемые среднесуточные нормы потребления магния приведены в табл. 1. Поступающий с водой и продуктами питания ионизированный магний попадает в желудок, где происходит отщепление части ионов магния от магнезиальных солей пищи и всасывание в кровь. Всасывание магния может увеличиваться в присутствии витамина В и некоторых органиче- 6 ских кислот (молочной, оротовой и аспарагиновой) [27]. Абсорбция магния в ЖКТ уменьшается при наличии в рационе питания большого количества белка и жира, так как с ними магний образует нерастворимые или труднорастворимые соединения. Всасывание магния уменьшается при избытке кальция и фосфатов. Основная часть труднорастворимых солей магния переходит в кишечник и после соединения с жирными кислотами всасывается в кровь. Эти комплексные соединения магния поступают в печень, где используются для синтеза биологически активных соединений.
В щелочной среде тонкой кишки всасывается 30% магния, при этом преимущественно пассивно, небольшая часть ионов – активно с использованием транспортной функции белка [7]. Магниевый баланс регулируется почками. Они могут реабсорбировать до 99% магния, профильтровавшегося через гломерулярную мембрану. За сутки с мочой выделяется до 100 мг магния. Потери магния с мочой возрастают под влиянием катехоламинов и кортикостероидных гормонов. При пониженном поступлении магния с пищей экскреция его почками снижается, а при избыточном – повышается [1]. Соединения магния, поступившие в кровь, распределяются в организме неравномерно: около 60% поступает в кости, мышцы, сердце, почки, 39% составляет внутриклеточная фракция и только 1% – внеклеточная фракция. Магний – макроэлемент, природный антагонист кальция и регулятор сосудистого тонуса, артериального давления и периферического кровообращения. Общее содержание магния в организме составляет 21–28 г. В клетках ионы магния занимают второе место по содержанию после калия, при этом 80–90% ионов магния соединяются в комплексы с АТФ. Концентрация ионизированного магния в клетке поддерживается на постоянном уровне, несмотря на резкие колебания его внеклеточного содержания. Это происходит вследствие относительно ограниченной проницаемости плазматической мембраны для катиона и наличия системы транспорта магния в клетку для поддержания высокого трансмембранного градиента. В тканях с интенсивным обменом веществ (миокард, нервная ткань) отмечают наибольшее содержание магния [6]. Непосредственный признак внутри-клеточного дефицита магния – снижение его концентрации в сыворотке крови до уровня ниже 0,8 ммоль/л [11].
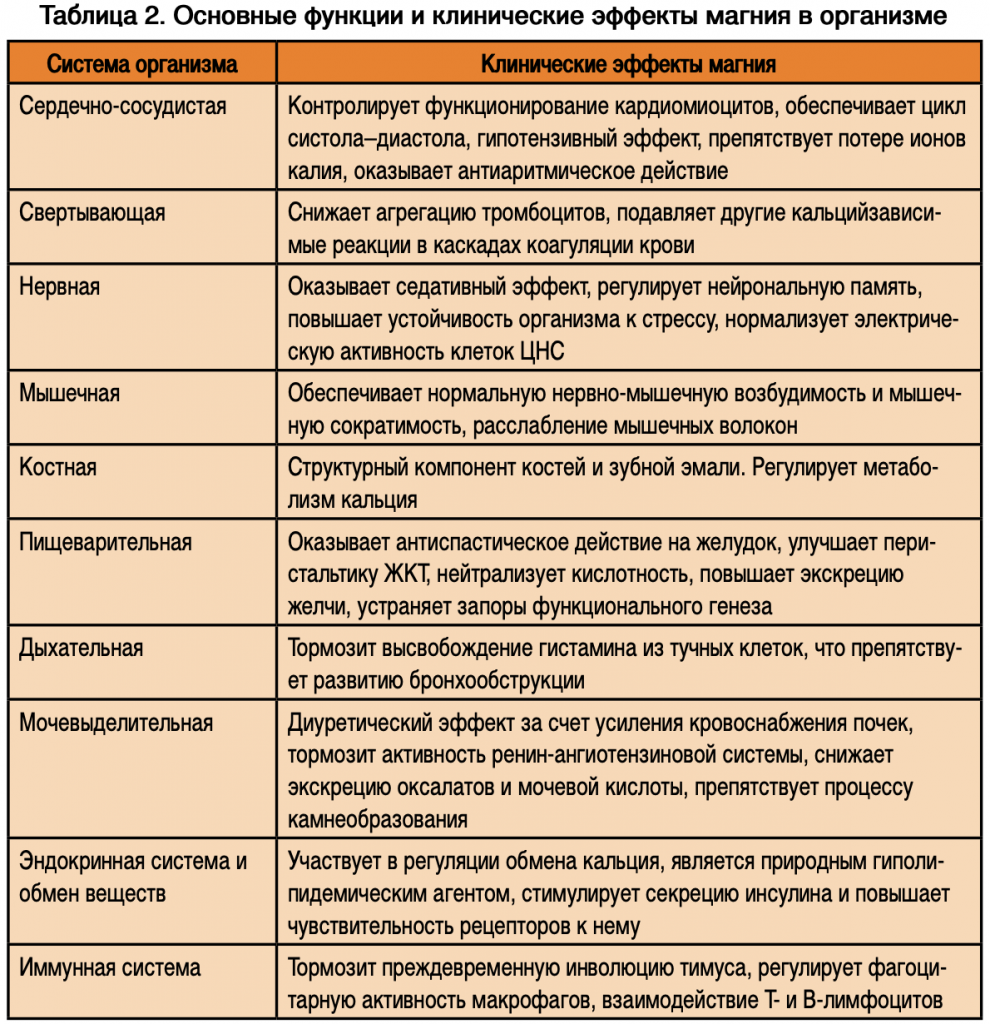
Дефицит магния – самый распространенный вид минеральной недостаточности у населения во многих странах, в частности в США. Так, исследования, проведенные в США в 1990-е гг., показали, что гипомагниемия встречается в 47,1% случаев, однако клинические признаки магниевого дефицита отмечались более чем у 72% взрослых американцев [28]. По результатам исследования уровня магния у 16 000 жителей Германии в 2001 г., субоптимальный уровень (ниже 0,76 ммоль/л) обнаружен у 33,7% обследованных [20]. По данным российских исследователей, распространенность дефицита магния в популяции составляет от 16 до 42% [9]. Магний, участвуя в обеспечении важнейших биохимических и физиологических процессов в организме, влияет на энергетический, пластический, электролитный обмены и в настоящее время рассматривается как один из важнейших внутриклеточных макроэлементов [2, 8]. Являясь универсальным регулирующим фактором, магний оказывает нормализующее влияние на функциональное состояние практически всех органов и систем в организме (табл. 2). Европейское ведомство по безопасности пищевых продуктов (EFSA) подтвердило факт улучшения состояния здоровья пациентов на фоне адекватного потребления магния с пищей за счет регуляции электролитного баланса, нормализации общего метаболизма, регуляции процесса деления клеток, сохранения состояния костной ткани, нормализации различных физиологических функций, снятия симптомов усталости, повышения выносливости [26].
Основные причины развития дефицита магния у детей:
– недостаточное поступление (диетические ограничения, термическая обработка продуктов, избыток углеводов, жиров, фосфатов и кальция в рационе, чрезмерное употребление кофе, сладких газированных напитков, регионы с «мягкой» водой);
– повышенная потребность (стресс, физическое перенапряжение, гиподинамия, эмоциональные нагрузки, периоды роста и после вирусных и бактериальных заболеваний);
– нарушение абсорбции магния в кишечнике, связанное с заболеваниями ЖКТ (хронический гастродуоденит, дисбактериоз кишечника, синдром мальабсорбции и др.);
– повышенное выведение почками при заболеваниях мочевой системы;
– нарушения регуляции обмена магния;
– эндокринная патология (гипертирео-идизм, гиперпаратиреоидизм, гиперальдостеронизм, диабет);
– терапия лекарственными препаратами (глюкокортикостероиды, цитостатики, аминогликозиды, фторхинолоны, сердечные гликозиды, мочегонные препараты, противоглистные препараты, фолиевая кислота, цианокобаламин);
– парентеральное питание.
Признаки гипомагниемии можно определить у ребенка по следующим проявлениям:
– синдром гиперактивного, «трудного» ребенка;
– повышенная утомляемость, раздражительность, состояние хронической усталости, депрессивные состояния, апатия, снижение памяти, головокружение, снижение способности сконцентрироваться и удерживать внимание;
– мышечные спазмы, судороги мышц, нарушение засыпания либо тревожный сон, зябкость (при отсутствии явных признаков других заболеваний);
– потеря аппетита, тошнота, рвота, склонность к поносам, запоры, потеря веса;
– иммунодефициты;
– кардиалгии, аритмии, колебания артериального давления.
Риск развития гипомагниемии резко увеличивается при:
– недостаточно разнообразной диете, содержащей мало нерафинированных злаковых и особенно зеленых, желтых, красных овощей и фруктов;
– диете с низким содержанием белков;
– частом употреблении кофе (более 2–3 чашек в день);
– употреблении алкоголя, в том числе напитков типа пива, «джинтоника»;
– применении наркотиков;
– курении;
– приеме мочегонных средств.
Рядом исследователей установлено, что при значительных учебных нагрузках и высокой ответственности ребенка, посещающего несколько школ, кружков, частом пребывании на шумных дискотеках со световыми и звуковыми эффектами, повышается расход магния в организме, и в случае недостаточного поступления иона с пищей развивается его дефицит [16]. Спортсмены также относятся к группе риска по развитию дефицита магния. Условия жизни спортсменов, включающие значительные физические и психоэмоциональные нагрузки, коррекцию массы тела в сторону увеличения либо снижения за короткие промежутки времени с использованием лекарственных препаратов (диуретики), значительную потерю иона магния с потоотделением, постоянную потребность в высокоэнергетическом питании, обусловливают повышенную потребность в магнии [5]. Дефицит магния часто сопровождает физические и психические стрессовые состояния. Повышение в крови содержания катехоламинов и стероидов при остром стрессе вызывает истощение внеклеточного и внутриклеточного пула магния, а также увеличивает его выделение с мочой, поскольку в стрессовой ситуации наблюдается повышение уровня адреналина и норадреналина. Дефицит магния не имеет патогномоничных клинических признаков. Однако полисимптомность этого состояния позволяет на основании клинической картины с большой долей вероятности заподозрить дефицит магния у больного [7].
Начальные признаки дефицита магния в организме проявляются:
– сердцебиением, аритмией, тахикардией, гипо- или гипертензией;
– нарушениями ритма сердца, синдромом вегетативной дисфункции;
– бессонницей, кошмарными снами, тяжелым пробуждением, плаксивостью или приступами тоски;
– состоянием беспокойства, тревожным возбуждением, нервозностью, страхом, нарушением кожной чувствительности (гиперестезией);
– быстрой утомляемостью, частыми головными болями, трудностями с концентрацией внимания; внезапными головокружениями, потерей равновесия, утренней усталостью, даже после долгого сна, ощущением тяжести в теле;
– выпадением волос, ломкостью ногтей, кариесом зубов;
– чувствительностью к изменениям погоды;
– сниженной температурой тела, холодными руками и ногами, покалыванием в ногах, спазмами;
– подергиванием век; туманом, мерцающими точками перед глазами;
– усиленным старт-рефлексом, нетерпением, желанием делать одновременно много дел, которые человек начинает и не заканчивает.
При прогрессировании гипомагниемии у пациентов выявляются:
– острые, спазматические боли в желудке, нередко сопровождающиеся поносом;
– функциональные и хронические заболевания ЖКТ;
– бронхоспазм, ларингоспазм;
– спазмы мышц, мышечные подергивания (тетания), тремор, боль при потягивании или напряжении мышц;
– анемия;
– образование камней в почках;
– обызвествление тканей, характерное для гиперкальциемии, но на фоне нормального содержания кальция;
– образование тимомы (увеличение размеров вилочковой железы), нарушение иммунитета.
Некоторые исследователи считают, что у детей с синдромом дефицита концентрации внимания с гиперактивностью (СДВГ) могут проявляться симптомы умеренной гипомагниемии: раздражительность, снижение устойчивости внимания. В ходе одного клинического исследования у 95% детей с указанным выше синдромом была выявлена гипомагниемия. В ходе другого клинического исследования у детей с СДВГ, которые получали магний, наблюдалось значительное улучшение поведения, в отличие от тех, кто получал стандартное медикаментозное лечение СДВГ без добавления магния [5]. На ЭКГ дефицит магния манифестируется замедлением атриовентрикулярной проводимости, уширением комплекса QRS, удлинением интервала QT, неспецифическим снижением интервала ST, уплощением зубца Т и формированием выраженной волны U. Дефицит иона магния достаточно значим, однако его диагностика представляет определенные трудности. Диагностировать дефицит магния не просто как по клиническим признакам, что связано с полисимптомностью проявлений, которые обусловлены участием микроэлемента в регуляции многих физиологических процессов человеческого организма, так и по анализу крови, который дает неполную информацию о содержании микроэлемента. Для оценки содержания магния в организме используют различные методики: внутриклеточное определение содержания магния в эритроцитах и мононуклеарах, исследование уровня магния в волосах, определение экскреции магния с мочой (нагрузочная проба), оценка концентрации магния в плазме крови (в норме – 0,8–1,2 ммоль/л). Наиболее распространено определение концентрации магния в плазме крови, однако его клиническое значение ограничено. Поскольку Mg2+ – внутриклеточный ион, его концентрация в сыворотке малоинформативна для оценки его общего количества в организме и диагностики наличия или отсутствия магниевого дефицита. При скрытом (внутриклеточном) дефиците этот показатель остается в пределах нормы [25]. Методы коррекции дефицита калия и магния включают в себя диетические мероприятия и фармакотерапию. Ежедневное поступление необходимого количества калия и магния можно обеспечить рациональным питанием. Фармакотерапия предусматривает три варианта минеральной коррекции – лечебную (заместительную), профилактическую и элиминационную (выведение избытка при гиперэлементозах) [6]. Лечебная стратегия используется при наличии отчетливых клинических или субклинических признаков гипоэлементозов. Правильная тактика заместительной терапии должна основываться не только на клинической картине дисбаланса микро- и макроэлементов, но и должна учитывать предварительную количественную оценку концентрации минералов в различных субстратах человека. Лечебная коррекция предусматривает использование более интенсивных и длительных курсов лечения. Профилактическая коррекция рекомендуется пациентам из группы риска по развитию гипоэлементозов при наличии у них минимальных клинических проявлений дефицита микро- и макроэлементов. Учитывая значимость ионов калия и магния в развитии патологии в организме, необходимость проведения коррекции калий-магниевого дефицита бесспорна. При этом сочетание ионов калия и магния в одном препарате предпочтительно, так как обосновано тем, что дефицит калия (особенно при заболеваниях ЖКТ) часто сопровождается дефицитом магния и требует одновременной коррекции содержания в организме обоих ионов. При одновременной коррекции уровней этих электролитов наблюдается аддитивный эффект. Существует достаточно большое число препаратов для восполнения недостаточности этих ионов. Однако это весьма затруднительно в связи с тем, что и калий, и магний представляют собой, как было отмечено выше, главным образом внутриклеточные ионы. Именно поэтому целесообразно использовать восполнение дефицита этих ионов компонентами, способствующими проникновению ионов калия и магния во внутриклеточное пространство или «выбирающих» оптимальное направление метаболических внутриклеточных процессов [12].
К компонентам, способствующим проникновению обсуждаемых ионов в клетку, можно, в частности, отнести аспарагинат. L-аспарагинат, связывая ионы металлов, через собственную транспортную систему переносит их внутрь клетки [21]. Именно L-аспарагинат, поступая в клетки, включается в процессы метаболизма [24]. Сама по себе аспарагиновая кислота принимает активное участие в аминокислотном обмене, являясь исходным материалом для синтеза заменимых аминокислот в организме, что следует учитывать при выборе препаратов для обеспечения нутриционной поддержки [4]. При этом смесь калиевой и магниевой солей аспарагиновой кислоты значительно повышает общую выносливость и активизирует анаболические процессы в мышечной ткани [19]. В настоящее время существует несколько препаратов, содержащих калий и магний, для заместительной терапии. Одним из наиболее эффективных препаратов является панангин, который, помимо калия и магния, содержит аспартат, обеспечивающий активный транспорт ионов калия и магния через мембрану клетки, влияя тем самым на осуществление нормального клеточного метаболизма, а также обеспечивает миоциты энергетическим субстратом для окислительного фосфорилирования [31].
Поэтому Панангин считается препаратом выбора в комплексном лечении и профилактике гипокалиемии и гипомагниемии. Кардио-протекторное действие, положительное влияние на функцию печени, снижение артериального давления и риска развития аритмии при приеме Панангина существенно расширяет спектр его клинического применения [28, 29]. Для профилактической коррекции гипокалиемии и гипомагниемии рекомендуется назначать Панангин по 1 таблетке 1–3 раза в день после еды в зависимости от возраста пациента (до 8–9 лет – по 1 таблетке, с 10 до 14 лет – по 2 таблетки, с 15 лет – по 3 таблетки в сутки). Длительность курса лечения определяется индивидуально и обычно составляет 3–4 недели, что обусловлено медленным насыщением тканевых депо. В заключение следует заметить, что субклинические и манифестные гипокалиемия и гипомагниемия в клинической практике очень распространены, но часто остаются нераспознанными. Врач любой специальности должен постоянно помнить о клинических проявлениях дефицита калия и магния в организме, чтобы своевременно предупредить их, назначив адекватную терапию.
1. Агаджанян Н.А., Тель Л.З., Циркин В.И., Чеснокова С.А. Физиология человека. – Спб., 1998. – 528 с. 2. Андрианова М.Ю., Дементьева И.И., Мальцева А.Ю. // Анестезиология и реаниматология. – 1995. – № 6. – С. 73–76. 3. Булдакова Н.Г. //Рус. мед. журнал. – 2008. – № 29. –С. 1956–1958. 4. Городецкий В.В., Талибов О.Б. Препараты магния в медицинской практике. Малая энциклопедия магния. – М., 2003. – 44 с. 5. Громова O.A. Элементный статус у детей с различными последствиями перинатального поражения ЦНС: автореф. дис. …д-ра мед. наук. – Иваново, 2001. – 42 с. 6. Громова O.A., Никонов A.A. // Журн. неврологии и психиатрии им. С.С. Корсакова. – 2002. –№ 12. – С.45–49.