Обратная зависимость между потреблением магния и кальцинозом коронарных артерий
Адела Хруби (Adela Hruby), д-р фил., магистр обществ. здравоохр.,* Кристофер Дж. О’Доннелл (Christopher J. O'Donnell), врач, магистр обществ. здравоохр.,†‡§ Поль Ф. Жак (Paul F. Jacques), д-р наук,*

Кальциноз коронарных артерий (ККА) (1-3) и брюшной аорты (КБА) (3-5) является признаком прогрессирующего атеросклероза, и прогностическим фактором сердечно-сосудистых заболеваний (ССЗ) и смертности от них, независимо от традиционных факторов риска ССЗ. В частности, было установлено, что определение степени ККА позволяет различить и пересмотреть категорию риска развития клинически значимых коронарных событий (6). Потребление магния, который содержится во многих продуктах питания, включая цельные злаки, зеленые листовые овощи, миндаль, кофе и темный шоколад, связано с многими аспектами здоровья сердечно-сосудистой системы (7-9), и этот микроэлемент играет ключевую роль в предотвращении кальциноза сосудов. Профилактическая роль магния в отношении кальциноза может объяснить ранее сделанные наблюдения, что повышенное потребление магния сопровождается снижением риска инсульта (10,11), нефатального инфаркта миокарда (ИМ) внезапной сердечной смерти и фатальной ишемической болезни сердца (ИБС) (12-14).
СОКРАЩЕНИЯ И УСЛОВНЫЕ ОБОЗНАЧЕНИЯ
КБА ― кальциноз брюшной аорты
ША ― шкала Агатстон
ККА ― кальциноз коронарных артерий
ХБП ― хроническая болезнь почек
КТ ― компьютерная томография
ТСПН ― терминальная стадия почечной недостаточности
СКФ ― скорость клубочковой фильтрации
ТИМ ― толщина комплекса интима-медиа
МДКТ ― субисследование с мультидетекторной компьютерной томографией Фрамингемского исследования сердца
СПВ ― скорость пульсовой волны
В экспериментах in vitro (15-19) и в исследованиях на животных (19-23) выявлены возможные биологические механизмы, посредством которых магний может предотвращать образование или вызывать обратное развитие бляшек и их кальцификации. Магний может выступать в роли антагониста кальция (24) и непосредственно подавлять осаждение гидроксиапатита и кристаллов (25-27). У пациентов с хронической болезнью почек (ХБП), терминальной стадией почечной недостаточности (ТСПН) или находящихся на гемодиализе ― у которых, как известно, ускоряется кальциноз ― наблюдалась обратная зависимость между концентрацией магния в сыворотке крови и степенью кальциноза в различных участниках сосудистого русла (27), а также связанными с ним показателями атеросклероза и артериосклероза, такими как толщина комплекса интима-медиа (ТИМ) и скорость пульсовой волны (СПВ) (17).
Наблюдательные исследования в общей популяции здорового населения также показали наличие обратной зависимости между концентрацией магния в сыворотке крови и ТИМ, наличием атеросклеротических бляшек и прогрессированием атеросклероза (28,29).
Однако, было показано, что концентрация магния в сыворотке крови слабо коррелирует с уровнем потребления магния (30,31). Только в одном наблюдательном исследовании изучалась связь между потреблением магния и степенью ККА у практически здоровых лиц, и его результаты не показали наличия этой связи (32). Ни в одном исследовании не изучалась связь между потреблением магния и степенью КБА. Таким образом, мы проверили гипотезу, что повышенное потребление магния ассоциировано с более низкой степенью кальциноза коронарных артерий и брюшной аорты у практически здоровых лиц, проведя кросс-секционную оценку зависимости между общим потреблением магния и степенью ККА и КБА в выборке участников, проживающих вне домов престарелых и не имеющих клинических признаков ССЗ.
Методы
Исследуемая выборка. Исследование FHS (Фрамингемское исследование сердца), проводимое под эгидой Национального института болезней сердца, легких и крови ― это продольное наблюдательное исследование компактно проживающего населения, начатое в 1948 г. в городе Фрамингеме, штат Массачусетс. Дети и супруги детей первоначальных участников когорты исследования FHS («Потомки», включенные в исследование в 1971–1975 гг.) проходят обследование в рамках последующего наблюдения по стандартным протоколам приблизительно 1 раз в 4 года (33). Когорта третьего поколения (включение участников с 2002 по 2005 гг.) охватывает 4095 детей из когорты «Потомков» (34). В настоящее исследование включены данные о рационе питания и факторах риска для участников из когорты «Потомков», прошедших обследование №7 (с 1998 по 2001 гг.; n = 3,539) и для участников из когорты «Третьего поколения», прошедших обследование №1 (с 2002 по 2005 гг.; n = 4095), а также принявших участие в обследовании №1 (с 2002 по 2005 гг.) в рамках участия в субисследовании с мультидетекторной компьютерной томографией (МДКТ). Как уже было описано ранее (35), 3529 участников из когорт «Потомков» и «Третьего поколения», проживающих на более обширной территории Новой Англии, прошли МДКТ сканирование. Мужчинам было ≥ 35 лет, женщинам ― ≥ 40 лет и они не были беременны; все участники весили ≤ 350 фунтов (159 кг) (35).
Мы исключили из анализа участников, у которых КТ снимки отсутствовали или не подлежали интерпретации (n = 278); имелись клинические признаки ССЗ (n = 136), а именно, проведение АКШ, протезирования клапана, чрескожной коронарной ангиопластики со стентированием, постановка искусственного водителя ритма, перенесенный инсульт, ИМ, ХСН или коронарная недостаточность, выявленные или развившиеся до даты клинического обследования (35); отсутствовали или были недостоверными сведения о рационе питания (n = 172, суточная калорийность составляла < 600 или ≥ 4000 ккал для женщин, < 600 или ≥ 4200 ккал для мужчин или было ≥ 12 незаполненных пунктов опросника); отмечались крайние уровни потребления магния или кальция (n = 48, уровень потребления попадал в 0,5-й или 99,5-й перцентиль); отсутствовала полная информация обо всех ковариатах (n = 200, определение см. ниже). После всех исключений объем выборки для настоящего анализа составил 2695 участников.
Протоколы сбора первичных данных были утверждены Экспертными советами Бостонского университета и Центральной больницы штата Массачусетс, Бостон, Массачусетс, а все участники предоставили письменное информированное согласие. Протокол настоящего исследования был рассмотрен Экспертным советом Университета Тафтса.
Оценка рациона. Для оценки потребления магния с продуктами питания использовался Гарвардский полуколичественный опросник частоты потребления различных пищевых продуктов (ОПП) из 126 пунктов (36). ОПП отправляли участникам по почте перед каждым обследованием и просили взять с собой заполненный ОПП на визит. Относительная надежность ОПП была показана в аналогичных выборках, так, корреляция между данными по общему потреблению магния, на основании сведений, предоставленных участниками с помощью ОПП и дневников питания, составляет 0,69–0,72 (36). Концентрацию магния в сыворотке крови – биомаркер содержания магния в организме, измеряли только в когорте «Потомков» в ходе обследования №2 (1979–1982 гг.), приблизительно за 20 лет до субисследования МДКТ, а в когорте «Третьего поколения» определение биомаркеров не проводилось. Таким образом, в данном анализе мы не оценивали концентрацию магния в сыворотке крови в качестве фактора воздействия.
Оценки исходов. Степень ККА и КБА количественно определяли по КТ-снимкам с помощью модифицированной шкалы Агатстон (ША), как описано ранее (35,37). Каждому участнику проводили МДКТ сканирование в на 8-срезовом аппарате, включавшее 2 снимка грудной клетки и 1 снимок брюшной полости («Лайтспид Ультра», Медицинские системы «Дженерал Электрик» Милуоки, Висконсин), в течение одной задержки дыхания на высоте вдоха. Для определения степени ККА было получено 48 смежных срезов толщиной 2,5 мм на каждом снимке. Для определения степени КБА в качестве нижней границы брюшной полости, подлежащей сканированию, выбрали уровень тела позвонка S1 и получили 30 смежных срезов толщиной 5 мм на участке 15 см выше S1. Очаги кальциноза определялись как участок ≥ 3 соединенных пикселей с ослаблением плотности КТ > 130 единиц Хаунсфилда. Оценку по ША рассчитывали путем умножения площади каждого очага на взвешенную оценку ослабления в зависимости от максимального ослабления в каждом очаге. Мы определяли наличие любой степени ККА или КБА при оценке по ША > 0, а высокую степень ККА (35) и высокую степень КБА (37) ― в соответствии с предварительно заданными отсечками 90-го перцентиля для возраста и пола относительно контрольной выборки здоровых лиц, участвующих в исследовании FHS.
Ковариаты. В ходе опроса каждого участника были получены сведения о возрасте, статусе курения, степени физической активности, уровне образования, приеме аспирина, гиполипидемических препаратов (напр., ниацина, фибратов, статинов), препаратов для лечения остеопороза (напр., препаратов кальцитонина, селективных модуляторов эстрогеновых рецепторов и других препаратов, влияющих на структуру и минерализацию костной ткани, включая бисфосфонаты, комбинации бисфосфонатов и костные морфогенетические белки), для лечения артериальной гипертензии и профилактики ССЗ (напр., ингибиторов АПФ, нитроглицерина, блокаторов кальциевых каналов, бета-адреноблокаторов), для лечения сахарного диабета (пероральных сахароснижающих препаратов или инсулина), наличии менопаузы и применении эстрогенной или другой заместительной гормональной терапии (ЗГТ) у женщин. У женщин наличие менопаузы определяли как отсутствие менструаций в течение >1 года. Индекс массы тела (ИМТ) рассчитывали как отношение массы тела в килограммах к квадрату роста в метрах. Артериальное давление измеряли дважды и рассчитывали средние показатели систолического и диастолического артериального давления (САД и ДАД, соответственно). Концентрацию общего холестерина измеряли энзиматическими методами, а фракцию ХС-ЛПВП измеряли после осаждения холестерина липопротеинов низкой плотности и очень низкой плотности. Концентрацию глюкозы в плазме крови натощак определяли в свежих образцах крови гексокиназным методом. Концентрацию инсулина в плазме крови натощак в когорте «Потомков» измеряли методом радиоиммунного анализа, разработанного для применения у человека, а в когорте «Третьего поколения» ― методом твердофазного иммуноферментного анализа (стандартизированного по анализу в когорте «Потомков»). Сахарный диабет 2 типа диагностировали при выявлении концентрации глюкозы натощак ≥ 126 мг/дл или на основании сведений о применении пероральных сахароснижающих препаратов или инсулина. С-реактивный белок (СРБ) в сыворотке крови измеряли с помощью усиленной частицами иммунонефелометрии с применением высокочувствительного реагента СРБ. Скорость клубочковой фильтрации (СКФ) рассчитывали по упрощенной формуле MDRD (исследование модификации диеты при поражении почек) с использованием концентрации креатинина в сыворотке крови, измеренной модифицированным методом Яффе (38).
Методы статистического анализа. Все количественные оценки потребления питательных веществ, полученные по результатам анализа заполненных участниками ОПП, были скорректированы с учетом общей калорийности рациона с помощью остаточного метода (39). Для представления характеристик участников и использования в регрессионном анализе были выделены квартильные категории общего потребления магния с поправкой на калорийность рациона. Линейные тенденции средних значений или процентов в характеристиках участников с поправками на возраст и пол (на возраст, пол и общую калорийность ― для нутриентов) в квартильных категориях оценивались с использованием медианы величины потребления в каждой категории.
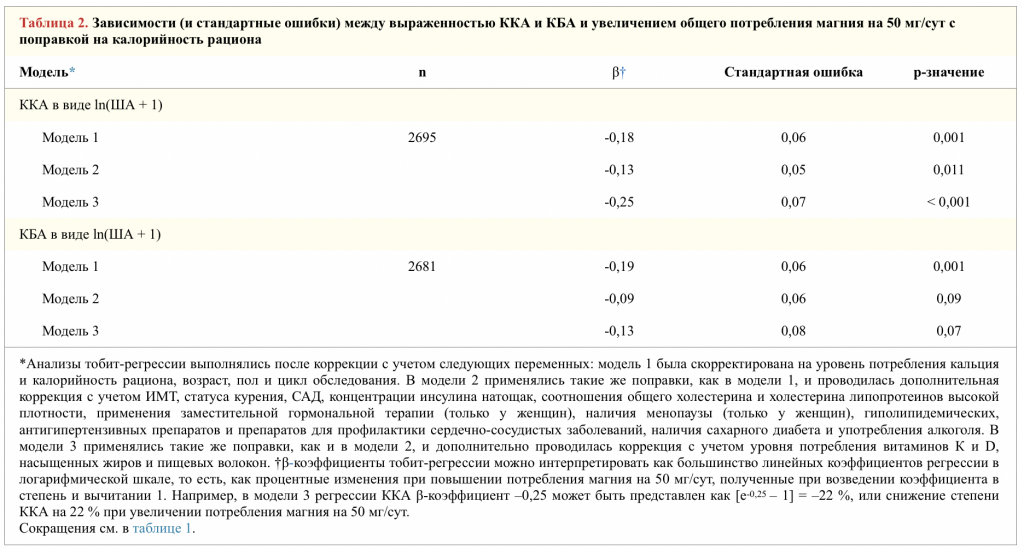
Мы использовали логарифмически (ln) преобразованные величины ККА и КБА после добавления единицы к каждой оценке в связи с большим количеством нулевых значений и для уменьшения асимметрии. Тобит-регрессия является оптимальной моделью для анализа данных по кальцинозу (40) и применялась в наших основных оценках зависимости между ln(ККА + 1) или ln(КБА + 1) и непрерывной переменной потребления магния в качестве воздействия (PROC LIFEREG с цензурированным порогом нулевого ККА или КБА). Мы приводим бета-коэффициенты и стандартные ошибки на каждые 50 мг общего потребления магния в сутки. Для анализов квартильных категорий мы приводим скорректированные средние значения и стандартные ошибки ln(ККА + 1) или ln(КБА + 1) в регрессии методом наименьших квадратов (PROC GLM) и р-значения для линейной тенденции в квартильных категориях общего потребления магния.
В модели регрессии были включены известные или потенциальные искажающие факторы, а именно: модель 1 анализировалась после коррекции с учетом возраста на момент исследования МДКТ (в годах), пола, цикла обследования, калорийности рациона (ккал/сут) и уровня потребления кальция (мг/сут). В модели 2 использовались такие же поправки, как в модели 1, и еще
учитывались известные факторы риска ССЗ, которые также могут опосредовать зависимость между рационом питания и кальцинозом, в том числе, ИМТ (кг/м2), статус курения (никогда/ранее/в настоящее время), соотношение общего холестерина и холестерина ЛПВП, концентрация инсулина натощак (ln-пмоль/л), САД (мм рт.ст), прием эстрогенов или ЗГТ в постменопаузе (у женщин, да/нет) и препаратов для лечения АГ или профилактики ССЗ, а также гиполипидемических или сахароснижающих препаратов (да/нет для всех) и употребление алкоголя (г/сут). В модели 3 (скорректированной с учетом всех переменных) применялись такие же поправки, как в модели 2, и дополнительно учитывались факторы питания, связанные с ССЗ или участвующие в развитии кальциноза, а именно, потребление пищевых волокон (г/сут), насыщенных жиров (г/сут), витамина D (МЕ/сут) и витамина К (мкг/сут). Дальнейшие поправки модели 3 на концентрацию СРБ (мг/л), регулярный прием аспирина (да/нет), СКФ (мл/мин/1,73 м2), уровень физической активности (ч/сут), прием препаратов для лечения остеопороза (да/нет), уровень образования (не учился в школе, окончил 1–8 классов; окончил 9–11 классов; окончил колледж или профессиональное училище; учился в вузе; окончил 2 курса вуза; получил степень бакалавра; окончил вуз или имеет профессиональную степень) или степень КБА (в виде ln[ША + 1], только в анализе ККА) существенно не повлияли на результат (данные не приведены). Кроме того, анализы, в которых было учтено влияние семейного анамнеза, не привели к значимым изменениям результатов; поэтому мы приводим результаты без поправок на эти взаимосвязи. Мы оценили потенциальную модификацию эффекта между общим потреблением магния и общим потреблением кальция, полом, ИМТ и возрастом, проведя тест на статистическое взаимодействие с помощью векторных произведений в анализах тобит-регрессии. Поскольку статистически значимых взаимодействий не наблюдалось (все p-значения > 0,05), эффекты взаимодействия были удалены из моделей, а ковариаты оставлены. Однако, в связи с различиями в распределении ККА по полу, мы повторили анализы у мужчин и женщин отдельно, с использованием квартильных категорий общего потребления магния с поправкой на калорийность рациона, и привели результаты этого поискового анализа в онлайн-приложении.
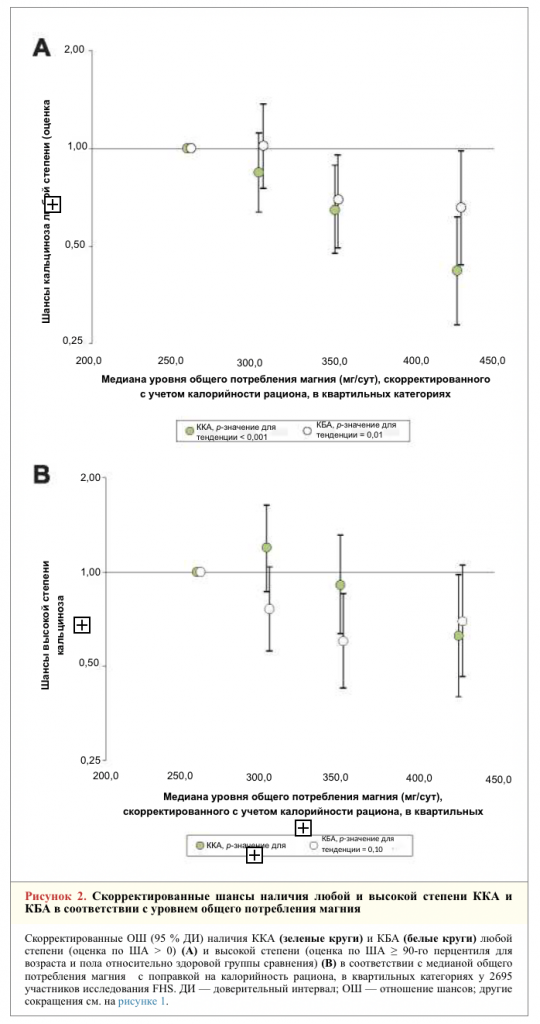
В дополнительных анализах для сравнения с опубликованными данными мы оценили шансы развития любой степени ККА или КБА (оценка по ША 0 или > 0), а также ККА или КБА высокой степени (оценка по ША < или ≥ 90-го перцентиля для возраста и пола по сравнению с контрольной группой [35,37]). Мы приводим отношения шансов (ОШ) и 95 % доверительные интервалы (ДИ) в каждой квартильной категории общего потребления магния с поправкой на калорийность рациона и р-значения для линейной тенденции между категориями. Категория самого низкого уровня потребления использовалась как категория сравнения.
Все анализы были проведены с использованием программного обеспечения SAS версии 9.3 (SAS Institute Inc, Кэри, Северная Каролина). Двустороннее р-значение < 0,05 расценивалось как статистически значимое по причине корреляции между двумя основными оцениваемыми исходами ― непрерывными показателями ККА и КБА.
Результаты
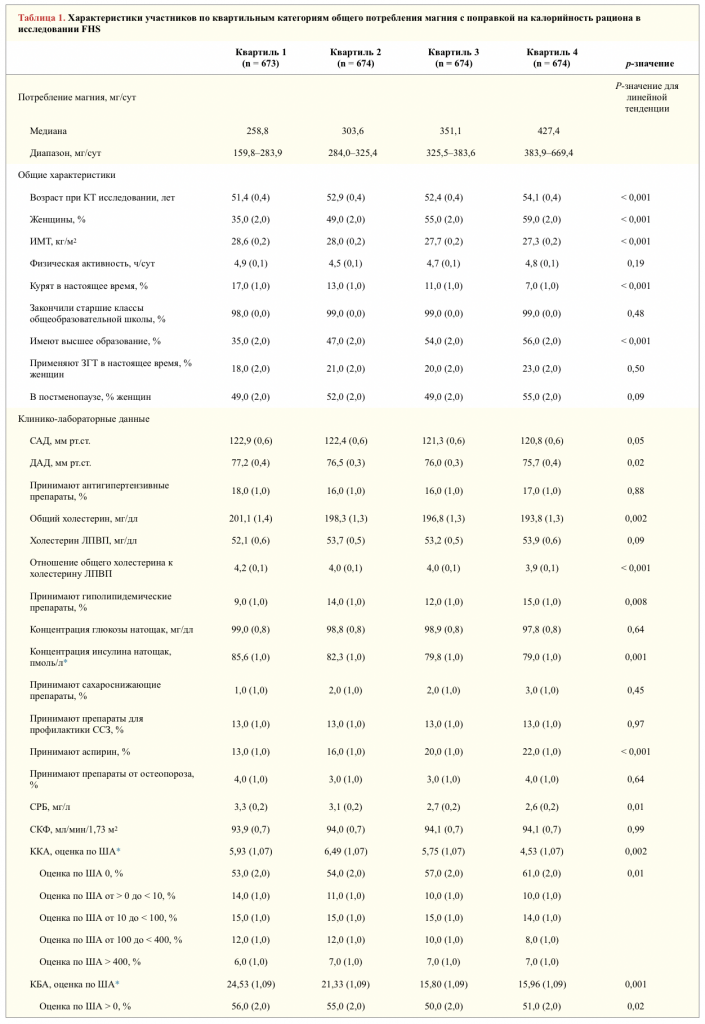
Клинические характеристики и особенности питания участников по квартильным категориям общего потребления
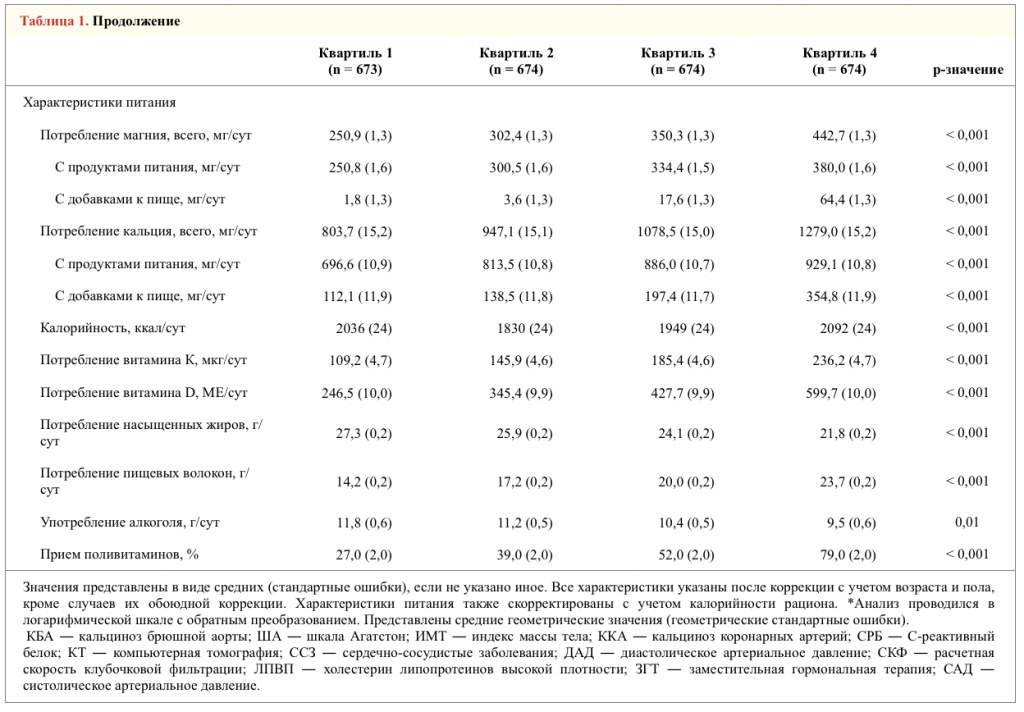
магния с поправкой на калорийность рациона представлены в таблице 1. Средний скорректированный уровень общего потребления магния составил 338 мг/сут. В среднем, дополнительные источники магния, по результатам опроса участников, составляли всего 6,4 % и 4,6 % общего потребления магния у женщин и мужчин, соответственно. По данным анализа тенденций в категории самого высокого уровня общего потребления магния было больше женщин, а также был выше процент лиц более старшего возраста, с более высоким уровнем образования, более низкими значениями ИМТ, ДАД, уровня общего холестерина, соотношения общего холестерина и холестерина ЛПВП, уровня инсулина натощак, СРБ и в целом с более полезным для здоровья рационом. Участники из этой категории чаще принимали гиполипидемические препараты и аспирин, а также реже курили на регулярной основе в течение прошлого года.
Основные анализы. ККА был выявлен (оценка по ША > 0) у 43,7 % участников (33,7 % женщин и 53,7 % мужчин). Распространенность КБА была выше: у 52,9 % участников определялась та или иная степень КБА (оценка по ША > 0), а различий по частоте его встречаемости в зависимости от пола выявлено не было (50,9 % женщин и 55,3 % мужчин). Среди участников с наличием любой степени КБА у 65,3 % выявлялся и ККА (у 55,3 % женщин и 74,3 % мужчин с КБА был выявлен ККА).
В модели, скорректированной с учетом всех переменных (модель 3), более высокий уровень общего потребления магния сопровождался снижением частоты ККА на 22 % при повышении уровня потребления на 50 мг/сут (таблица 2). Уровень общего потребления магния был достоверно связан со снижением степени КБА на 17 % в базовой модели (модель 1, p = 0,001), но эта связь ослабевала после коррекции с учетом факторов риска (модель 2, мощность 9 %; p = 0,09) и уровня потребления витаминов D и К, насыщенных жиров и пищевых волокон (модель 3, мощность 12 %; p = 0,07). В поисковых анализах, проведенных отдельно для каждого пола, обратная зависимость оказалось более выраженной у женщин, чем у мужчин, для обоих непрерывных исходов, хотя тесты на взаимодействие с полом не были статистически значимы (таблица 1 онлайн).
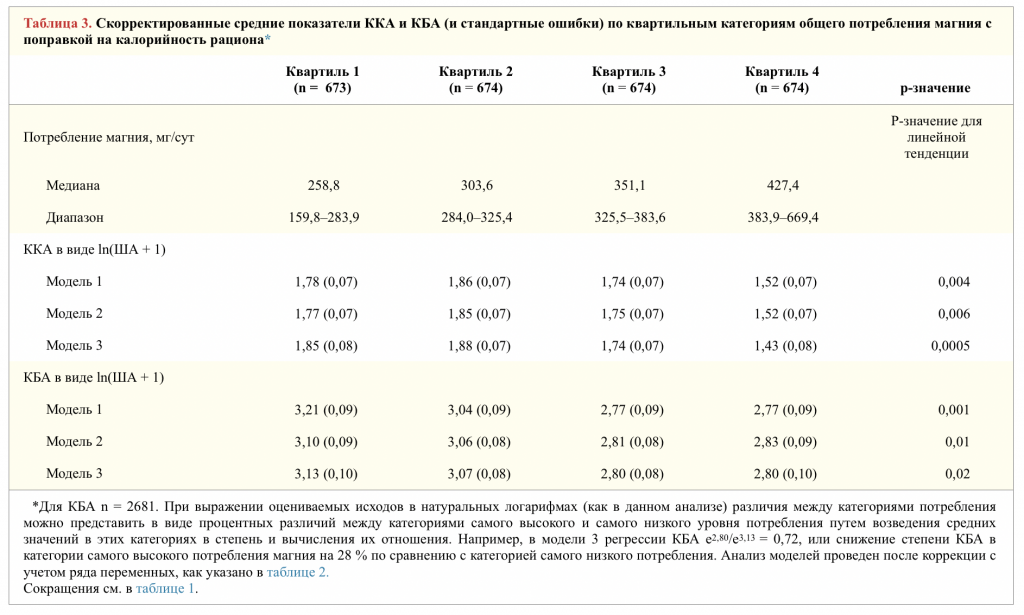
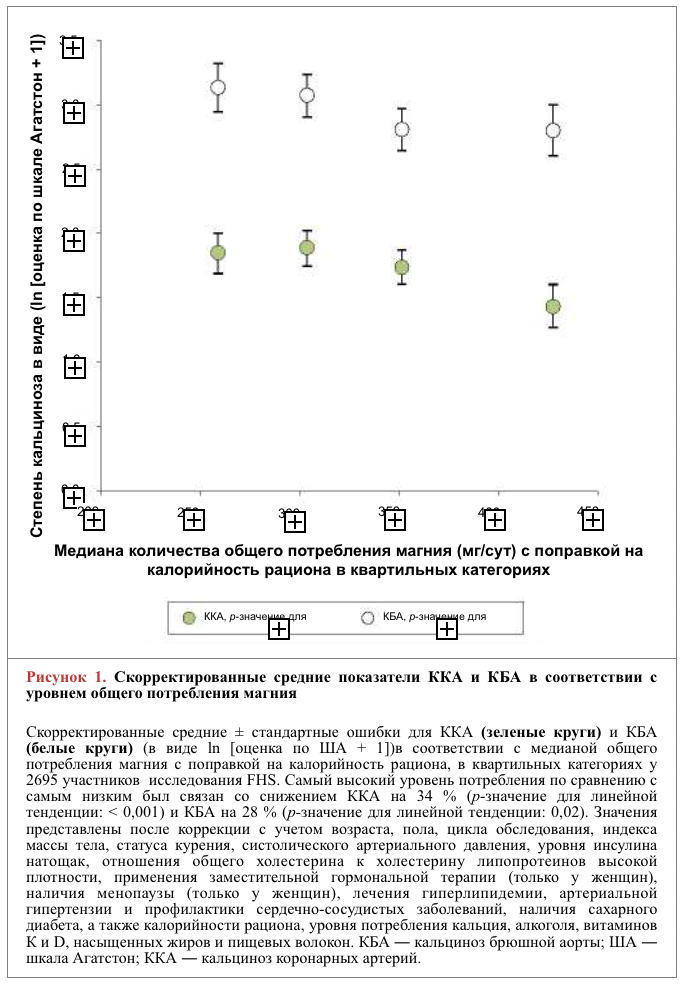
Тенденции средних степеней ККА и КБА в квартильных категориях уровня общего потребления магния совпадали с результатами тобит-регрессионного анализа (таблица 3, рис. 1 ― объединенный анализ; таблица 2 онлайн и рис. 1 онлайн ― отдельный анализ для каждого пола).
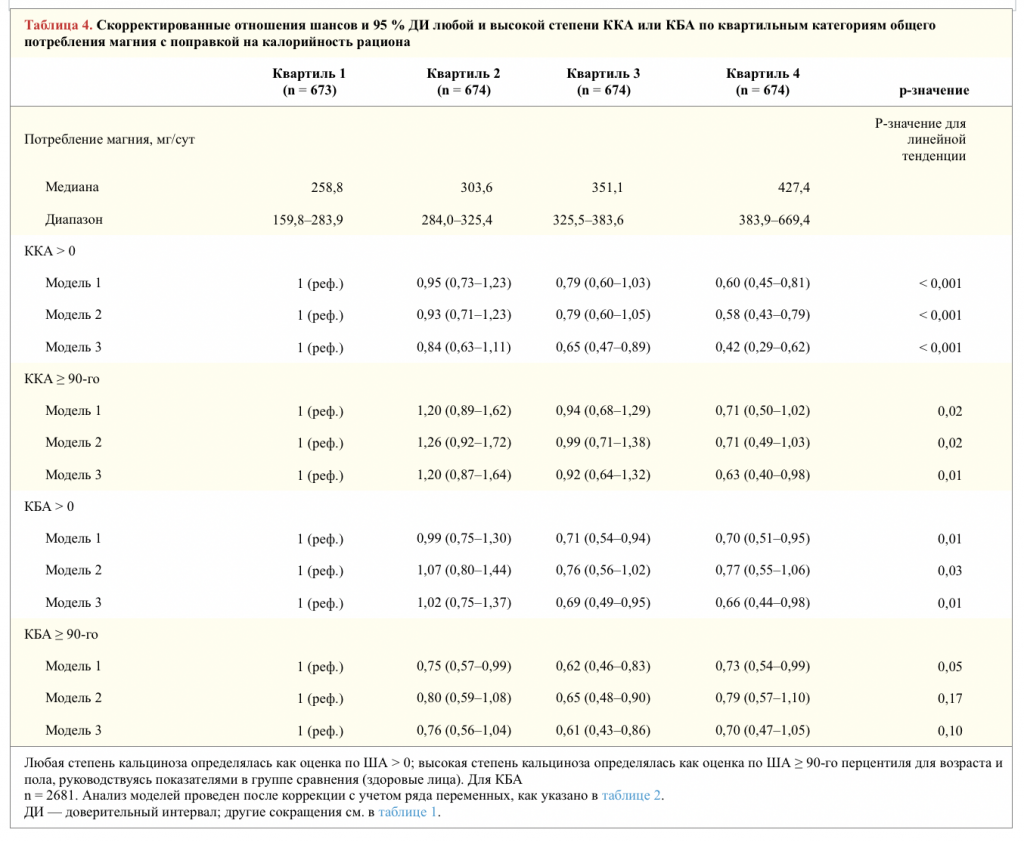
Дополнительные анализы. Мы изучили зависимость между уровнем общего потребления магния и шансами развития кальциноза любой степени (оценка по ША > 0) и высокой степени (оценка по ША ≥ 90-го перцентиля для пола и возраста) в брюшной аорте и коронарных артериях (таблица 4, рис. 2). В моделях, скорректированных с учетом всех переменных, у лиц из категории самого высокого потребления магния сравнению с самым низким его потреблением, шансы развития ККА любой степени были на 58 % ниже, ККА высокой степени ― на 37 % ниже, а шансы развития КБА ― на 34 % ниже. Наблюдалась незначимая обратная зависимость между высоким потреблением магния и шансами развития КБА высокой степени. Поисковый анализ, проведенный отдельно для каждого пола выявил аналогичные, статистически значимые зависимости для ККА любой степени у мужчин и женщин. Линейные тенденции для шансов развития ККА высокой степени, КБА любой и высокой степени не были статистически значимы ни для одного пола (таблица 3 онлайн, рис. 2 и 3 онлайн).
Обсуждение
Главный вывод, который позволяют сделать результаты данного исследования, заключается в том, что у лиц без клинически выраженных проявлений ССЗ более высокий уровень общего потребления магния связан с меньшей выраженностью ККА (чувствительный дифференцирующий показатель субклинических ССЗ), и меньшим общим бременем атеросклероза артерий. У лиц с самым высоким уровнем потребления магния вероятность выявления ККА была приблизительно вдвое меньше, чем у лиц с самым низким уровнем потребления, что указывает на возможную профилактическую роль потребления магния в замедлении развития кальциноза. Выявленные зависимости для ККА сохраняли значимость после проведения коррекции с учетом ряда кардиометаболических факторов риска и возможных опосредующих факторов, а также после дальнейшей коррекции с учетом степени КБА. Это может означать, что магний оказывает специфическое воздействие на коронарные артерии помимо его известных противовоспалительной, гипотензивной и антидислипидемической функций, влияющих на формирование кальциноза (7-9).
На сегодняшний день, только в одном кросс-секционном анализе, проведенном в исследовании MESA (многонациональное исследование атеросклероза [Multi-Ethnic Study of Atherosclerosis]), изучалась связь между уровнем потребления магния (по результатам опроса участников) и ККА. Хотя в указанном исследовании не было выявлено значимой зависимости между
уровнем потребления магния, по результатам опроса, и ККА, авторы установили, что более высокий уровень потребления магния был связан с более низкими шансами увеличения ТИМ коронарных артерий (32) – показателя атеросклеротического процесса, характеризующегося умеренной корреляцией с ККА. Некоторые различия между нашим анализом и исследованием MESA, которые могут объяснить несовпадение результатов, включают различия в выборках (широкое разнообразие расовой/этнической принадлежности в исследовании MESA; преимущественно европеоидная раса во Фрамингемском исследовании), учет уровня потребления кальция в качестве искажающего фактора в нашем анализе, а также применение пороговых значений ККА (> 0 или > 100) в исследовании MESA вместо оценки этого показателя как непрерывной переменной. Кроме того, мы не оценивали ТИМ или другие показатели бляшек в нашем исследовании, и, соответственно, не можем комментировать зависимость между потреблением магния и формированием атеросклеротических бляшек, а также не можем исключить дополнительную роль магния
в формировании бляшек отдельно от кальцификации бляшек, что также было показано в некоторых исследованиях на животных и клетках (21,22).
В нескольких исследованиях изучалось включение в рацион питания продуктов с высоким содержанием магния ― шоколада (41), кофе (42,43), рыбы (44) и цельных злаков (45) по отношению к влиянию на ККА, и были получены согласующиеся результаты. В Семейном исследовании сердца [Family Heart Study] наблюдалась обратная зависимость между уровнем потребления шоколада и шансами развития ККА (оценка по ША > 100) с дозозависимым ответом (41). В Роттердамском исследовании отмечалась обратная зависимость между более высоким уровнем потребления кофе и выраженным ККА у женщин старшего возраста, в отличие от мужчин (43). У более молодых лиц (от 18 до 30 лет) не было выявлено связи между потреблением кофе и наличием или прогрессированием ККА в течение 15–20 лет (42). Потребление цельных злаков не было связано с ККА еще в одном исследовании MESA, несмотря на значимую обратную связь с другими факторами риска ССЗ (45). Наконец, исследователи из Роттердама установили, что у лиц, употребляющих больше рыбы, реже встречается ККА средней (оценка по ША от 11 до 400) и тяжелой степени (оценка по ША > 400), чем у лиц, не употребляющих рыбу, и эта зависимость не относилась к потреблению докозагексаеновой или эйкозапентаеновой кислот ― жирных кислот, c которыми часто связывается польза употребления рыбы для сердечно-сосудистой системы (44). Эти расхождения могут быть связаны с различиями между выборками исследований, различным вкладом рассматриваемых пищевых продуктов в общий уровень потребления магния и сложными взаимодействиями между продуктами питания. Изучения влияния магнийсодержащих добавок к пище на риск ККА с участием практически здоровых лиц еще не проводилось, и нам неизвестно об оценке ККА в качестве вторичной конечной точки в исследованиях магнийсодержащих добавок с другими первичными конечными точками. Однако в небольшом пилотном исследовании с участием пациентов с ТСПН, находящихся на хроническом гемодиализе, у которых отмечается особенно высокий риск быстрого прогрессирования кальциноза, было выявлено незначимое прогрессирование ККА всего на 8 % (по сравнению с 50 % в типичных случаях) в течение 18 месяцев на фоне приема двойной углекислой соли магния и кальция (приблизительно 700 мг/сут магния и 1200 мг/сут кальция) вместо стандартных фосфат-связывающих препаратов на основе кальция (46).
Насколько нам известно, в нашем исследовании впервые была изучена зависимость между уровнем общего потребления магния и КБА, который, как и ККА, является независимым прогностическим фактором развития ССЗ и смертности от них (3-5). Несмотря на некоторые патоморфологические различия (47), полагают, что ККА и КБА имеют одинаковую природу, и наличие КБА является надежным предиктором ККА. Мы не можем дать объяснение тому факту, что выявленные зависимости между уровнем общего потребления магния и кальцинозом брюшной аорты и коронарных артерий имели различную степень выраженности, кроме как предположить, что магний играет потенциально главную роль в пока неустановленном специфическом процессе, который в большей степени связан с кальцификацией атеросклеротических бляшек коронарных артерий. Изначально мы предполагали, что потребление магния будет одинаковым образом влиять на формирование ККА и КБА. Одна из гипотетических ролей магния в предотвращении биоминерализации внескелетных тканей состоит в подавлении образования гидроксиапатита, в котором магний дестабилизирует кристаллическую структуру и препятствует его осаждению (17,26,27). Кроме того, было показано, что магний подавляет остеогенную дифференцировку гладкомышечных клеток сосудов (15,16,48) и повышает экспрессию белков, подавляющих кальциноз, одновременно снижая активность протеинов внеклеточного матрикса (16), и предотвращая апоптоз клеток (15).
Поскольку современные технологии получения снимков КТ не позволяют различить кальциноз медии и интимы, мы не можем исключить наличие кальциноза медии в качестве возможного объяснения до некоторой степени различающихся зависимостей между ККА и КБА. Считается, что кальциноз медии, который развивается в случаях длительного нарушения метаболизма (напр., при сахарном диабете, ХБП), редко встречается в коронарных артериях (49), но более распространен в брюшной аорте при наличии небольших нарушений метаболизма или дисбаланса микроэлементов. Однако полученные нами результаты существенным образом не изменились после исключения участников с сахарным диабетом (5 % исследуемой выборки) или нарушением функции почек (2 % исследуемой выборки), и мы учитывали показатели гликемии при проведении анализа. Эти противоречия, а также роль потребления магния с продуктами питания в процессах специфической кальцификации атеросклеротических бляшек в коронарных артериях заслуживают дальнейшего изучения.
Ограничения исследования. По причине кросс-секционного анализа мы не можем сделать какие-либо выводы о зависимости наших наблюдений от времени. Хотя полученные нами результаты имеют вескую биологическую основу, механизмы выявленных зависимостей остаются неясными. Высокий уровень потребления магния может быть суррогатным маркером здорового образа жизни; в частности, повышенный уровень потребления магния коррелирует с меньшей частотой курения и более низким ИМТ, но при этом с более частым применением гиполипидемических препаратов и аспирина. Хотя мы учитывали особенности образа жизни, способные повлиять на развитие ССЗ или кальциноза (напр., курение, потребление кальция, пищевых волокон и насыщенных жиров, уровень физической активности, уровень образования), тем не менее, могут остаться неизвестные
искажающие факторы, как и в любом наблюдательном исследовании, и их влияние на степень достоверности наших наблюдений сложно оценить. Для подтверждения зависимости между уровнем потребления магния и степенью кальциноза требуются продольные, а впоследствии рандомизированные исследования. Расчетные средние потребления кальция в категориях уровней потребления магния, по результатам опроса участников, были получены с помощью анализа линейной регрессии; и хотя в анализах тобит- и линейной регрессии были получены аналогичные оценки, представленные средние значения могут вести к переоценке или недооценке степени выявленной зависимости. Наконец, участники нашего исследования были преимущественно европеоидной расы; таким образом, полученные нами результаты могут не могут быть распространены на другие расы/этнические группы.
Выводы
Мы выявили сильную зависимость между повышенным уровнем общего потребления магния и более низкой степенью кальциноза коронарных артерий, являющегося важным показателем субклинического атеросклероза, и позволяющего пересмотреть риск развития ССЗ и смертности от них. Наши наблюдения указывают на то, что в будущих исследованиях можно рассматривать влияние магния на ККА как потенциальный физиологический механизм, посредством которого потребление магния с пищей снижает риск инсульта, нефатального ИМ и фатальной ИБС. В дополнение к будущим исследованиям влияния магния на количество и плотность очагов кальцификации и общее количество кальцифицированных и некальцифицированных бляшек, необходимы также проспективные исследования для изучения влияния магния на рассмотренные нами и другие участки кальциноза сосудов, а также возможной пользы приема магнийсодержащих добавок к пище для замедления начала и прогрессирования атеросклероза и кальциноза. Цель этих исследований должна состоять в установлении механизма влияния магния на снижение риска наступления сердечно-сосудистых событий и итоговое снижение бремени сердечно-сосудистых заболеваний.
Благодарности
Авторы благодарят Гейл Роджерс (Gail Rogers), магистра наук, за рецензию статистических методов и участников Фрамингемского исследования сердца за их вклад и участие в работе.
Запросы на перепечатку и корреспонденцию направлять: Д-р Никола М. МакКаун (Nicola M. McKeown), Программа эпидемиологии питания, Центр изучения питания и старения человека имени Джина Мэйера при Министерстве сельского хозяйства США в Университете Тафтса, 711 Вашингтон Стрит, 9-й этаж, Бостон, Массачусетс 02111. Адрес эл. почты: nicola. mckeown@tufts.edu.
*Программа эпидемиологии питания, Центр изучения питания и старения человека имени Джина Мэйера при Министерстве сельского хозяйства США в Университете Тафтса, Бостон, Массачусетс; †Национальный институт болезней сердца, легких и крови (NHLBI), отдел внутренних исследований, и Фрамингемское исследование сердца под эгидой NHLBI, Фрамингем, Массачусетс; отделение сердечно-сосудистых заболеваний, медицинский факультет, Центральная больница штата Массачусетс, Бостон, Массачусетс; §Гарвардская медицинская школа, Бостон, Массачусетс; отделение общей терапии, медицинский факультет, Центральная больница штата Массачусетс, Бостон, Массачусетс; Программа МРТ, ПЭТ, КТ сердца Центральной больницы штата Массачусетс и рентгенологическое отделение Центральной больницы штата Массачусетс, бостон, Массачусетс. На момент написания статьи д-р Хруби получала стипендию Американской кардиологической ассоциации для аспирантов. Данная работа также получила поддержку в рамках финансирования Фрамингемского исследования сердца от Национального института болезней сердца, легких и крови (контракт № N01- HC-25195) и Министерства сельского хозяйства США (соглашение № 58-1950-0-014). Д-р Жак был членом Консультативного совета по диетологии штата Массачусетс и Консультативного совета производителей йогурта «Данон». Д-р Мейгс получил поддержку от Национального института сахарного диабета, болезней пищеварительной системы и почек (NIDDK) (K24 DK080140). Все авторы заявили об отсутствии подлежащих раскрытию отношений, связанных с содержимым данной статьи.
Статья получена 16 августа 2013 г.; пересмотренная статья получена 25 октября 2013 г.; принята в печать 25 октября 2013 г.

